Interprétation des électrocardiogrammes néonatals et pédiatriques (ECG)
Définition de l’ECG pédiatrique et néonatal : normal et pathologique
L’électrocardiogramme (ECG) néonatal et pédiatrique, bien qu’interprété selon les mêmes principes fondamentaux que celui de l’adulte, présente des spécificités physiologiques majeures qui évoluent de la naissance à l’adolescence. Cette évolution reflète les changements hémodynamiques, notamment la transition de la circulation fœtale à la circulation néonatale et la maturation du système de conduction. L’ECG doit toujours être interprété selon une approche systématique rigoureuse, en tenant compte de l’âge précis du patient (en jours pour les nouveau-nés, en mois pour les nourrissons), afin de ne pas classer à tort une variante physiologique comme pathologique ou de manquer une anomalie subtile. Les paramètres suivants doivent être évalués, par ordre chronologique :
- Fréquence cardiaque
- Rythme et axe électrique
- Onde P (amplitude et durée)
- Intervalle PR
- Complexe QRS (morphologie, durée, voltage)
- Segment ST
- Onde T (axe et polarité)
- Onde U
- Intervalle QT (QTc)
Les électrocardiogrammes pédiatriques diffèrent nettement de ceux des adultes – en termes de fréquence, de morphologie des complexes, de dominance ventriculaire et de repolarisation. Il est essentiel de maîtriser les valeurs normatives (telles que les tables de Davignon ou de Rijnbeek), les variantes physiologiques et les signes d’appel pathologiques spécifiques aux nouveau-nés, aux nourrissons et aux enfants. Vous trouverez ci-dessous une discussion approfondie sur chacun des paramètres énumérés. La plupart des diagnostics mentionnés sont abordés en détail dans d’autres chapitres, vers lesquels des liens sont fournis.
Considérations techniques et placement des électrodes
La qualité du tracé est primordiale. Chez le nourrisson et le jeune enfant, la surface corporelle réduite impose une attention particulière au placement des électrodes pour éviter les chevauchements. De plus, en raison de la dominance ventriculaire droite physiologique à la naissance et durant la petite enfance, il est souvent recommandé d’enregistrer les dérivations droites (V3R et V4R) systématiquement chez le nouveau-né et le nourrisson, en plus ou à la place des dérivations gauches extrêmes (V7, V8), pour mieux explorer le ventricule droit.
Fréquence cardiaque
Au cours de la première semaine de vie, la fréquence cardiaque est d’environ 120 battements/min, mais peut osciller physiologiquement de manière importante. La fréquence cardiaque augmente ensuite au cours des 1 à 2 premiers mois pour atteindre un pic vers 150 battements/min. Elle diminue ensuite progressivement pour atteindre environ 120 battements/min à l’âge de 6 mois. Après l’âge de 12 mois, la fréquence cardiaque diminue régulièrement et, à l’âge de 10 ans, elle se rapproche des valeurs adultes. Ces variations sont dues à l’évolution du métabolisme basal, à la maturation du tonus vagal et à des modifications de l’automatisme du nœud sinusal. Il est crucial de noter que les enfants augmentent leur débit cardiaque principalement en augmentant leur fréquence cardiaque, le volume d’éjection systolique étant relativement fixe.
Le rythme
Rythme normal
Un rythme est défini comme une séquence de battements cardiaques organisés. Le nœud sinusal (SA) est le stimulateur cardiaque physiologique dominant. Le rythme sinusal est le rythme normal chez tous les patients pédiatriques. Il est défini par les critères suivants :
- Rythme régulier (ou phasique avec la respiration) avec une fréquence ventriculaire comprise dans l’intervalle normal spécifique à l’âge.
- Onde P de morphologie constante précédant chaque complexe QRS.
- L’onde P est positive dans la dérivation II, I et aVF (axe de P normal entre 0° et +90°).
Arythmies
Tachycardie sinusale
On parle de tachycardie sinusale lorsque la fréquence cardiaque dépasse la limite supérieure de la normale pour l’âge. Chez le nourrisson, elle peut atteindre ou dépasser 220 battements/min, tandis qu’elle peut dépasser 180 battements/min chez l’enfant plus âgé lors d’un effort intense. Comme dans le rythme sinusal de repos, une onde P précède chaque complexe QRS et l’axe de l’onde P reste normal.
La tachycardie sinusale est une réponse physiologique et non une arythmie primaire ; la cause sous-jacente doit toujours être recherchée. La douleur, l’anxiété, les infections, la fièvre, l’hypovolémie, la déshydratation, l’anémie, l’hyperthyroïdie, l’effet catécholaminergique (médicaments ou endogène) et la myocardite sont des étiologies courantes. Le traitement est étiologique.
Arythmie sinusale
L’arythmie sinusale (arythmie sinusale respiratoire) est extrêmement fréquente en pédiatrie et remplit tous les critères du rythme sinusal, à l’exception de la régularité stricte des intervalles R-R. Le phénomène s’explique par l’influence du cycle respiratoire sur le tonus vagal. La fréquence cardiaque s’accélère pendant l’inspiration (inhibition vagale) et ralentit pendant l’expiration (stimulation vagale).
L’arythmie sinusale est un signe de bonne santé cardiovasculaire (variabilité de la fréquence cardiaque). Les ondes P sont identiques et l’intervalle PR est constant. Elle est souvent plus marquée chez l’adolescent et le jeune adulte sportif. La disparition de l’arythmie sinusale lors de l’apnée ou de l’effort confirme sa nature bénigne.
Pause sinusale
La pause sinusale se manifeste par un allongement soudain de l’intervalle P-P non lié au cycle respiratoire. Environ la moitié des nouveau-nés prématurés et à terme présentent des pauses sinusales transitoires (Southall et al.). Chez l’adolescent, des pauses nocturnes sont fréquentes. Une pause est généralement considérée comme pathologique si elle dépasse 3 secondes chez l’enfant, ou si elle provoque des symptômes. Un dysfonctionnement du nœud sinusal (intrinsèque ou post-chirurgical, par exemple après une intervention de type Mustard, Senning ou Fontan) doit être évoqué si les pauses sont inappropriées ou symptomatiques.
Rythme auriculaire ectopique
Le rythme auriculaire ectopique provient d’un foyer auriculaire autre que le nœud sinusal. Il se caractérise par des ondes P d’axe anormal (ex: négatives en DII, DIII, aVF pour un foyer bas-situé). Les enfants en bonne santé surveillés par Holter ECG présentent souvent de courts épisodes de rythme auriculaire ectopique ou d’échappement jonctionnel, notamment durant le sommeil lorsque le tonus vagal prédomine.
Si la morphologie de l’onde P varie battement par battement (au moins 3 morphologies différentes), on parle de pacemaker auriculaire errant (fréquence < 100 bpm) ou de tachycardie auriculaire multifocale (MAT) si la fréquence est rapide (rare chez l’enfant, parfois associée à des pathologies pulmonaires).
Autres tachyarythmies
Les tachyarythmies pédiatriques nécessitent une distinction rapide entre complexes fins et larges. Voir Diagnostic et prise en charge des tachyarythmies.
Tachycardies supraventriculaires (TSV) : Ce sont les plus fréquentes (90%).
La Tachycardie par Réentrée Auriculo-Ventriculaire (TRAV) sur voie accessoire est le mécanisme prédominant chez le nourrisson et le jeune enfant. La Tachycardie par Réentrée Intranodale (TRIN) devient plus fréquente à l’adolescence.
Le flutter auriculaire et la fibrillation auriculaire sont rares sur cœur sain et doivent faire rechercher une cardiopathie congénitale, une cardiomyopathie ou des antécédents de chirurgie atriale (cicatrices).
La tachycardie ectopique jonctionnelle (JET) est une arythmie spécifique, souvent observée en post-opératoire de chirurgie cardiaque congénitale (ex: fermeture de CIV), caractérisée par une dissociation AV.
Tachycardies ventriculaires (TV) :
Toute tachycardie à complexes larges (QRS > 0,08s chez le nourrisson, > 0,12s chez l’enfant plus âgé) doit être considérée comme une TV jusqu’à preuve du contraire. Les causes incluent les canalopathies (syndrome du QT long, CPVT, Brugada), les cardiomyopathies (ARVC, hypertrophique), les myocardites, ou les causes toxiques/métaboliques.
Attention, une TSV avec aberration de conduction (bloc de branche fonctionnel) est possible mais reste un diagnostic d’exclusion en urgence.
Les fréquences cardiaques lors des tachyarythmies peuvent être impressionnantes : > 280-300 bpm chez le nourrisson en flutter 1:1 ou en TRAV. Une fréquence ventriculaire fixe autour de 300 bpm chez un nouveau-né doit faire évoquer un flutter auriculaire.
Administration de l’adénosine chez les patients pédiatriques
Dosage : adénosine intraveineuse (IV) ou intraosseuse (IO).
Dose initiale : 0,1 mg/kg en bolus flash (maximum 6 mg).
En cas d’échec après 1-2 minutes : seconde dose de 0,2 mg/kg (maximum 12 mg).
Technique : Utiliser un robinet à 3 voies pour faire suivre immédiatement le médicament d’un bolus de 5 à 10 ml de sérum physiologique (flush).
Précautions : Enregistrement ECG continu (papier ou numérique) indispensable pendant l’injection pour analyser le mode de réduction ou la dissociation AV transitoire. Avoir le chariot de réanimation à proximité.
L’adénosine bloque transitoirement la conduction du nœud AV. Elle est curative pour les tachycardies dépendantes du nœud AV (TRAV, TRIN) et diagnostique pour les autres (démasque l’activité auriculaire dans le flutter ou la tachycardie atriale).
Note pharmacologique : Réduire la dose (50%) chez les patients sous carbamazépine (potentialisation possible) ou dipyridamole, ou chez les greffés cardiaques (hypersensibilité du nœud sinusal/AV dénervé).
Cardioversion électrique synchronisée
Indiquée en urgence absolue si instabilité hémodynamique (choc, hypotension sévère).
Dose initiale : 0,5 à 1 J/kg. Si échec, augmenter à 2 J/kg. Une sédation doit être envisagée si l’état de l’enfant le permet.
Bradycardie sinusale
La bradycardie est le signe pré-terminal le plus fréquent en cas d’hypoxie ou de choc chez l’enfant. Contrairement à l’adulte, le débit cardiaque pédiatrique est très dépendant de la fréquence. Une fréquence < 60 bpm chez un nourrisson avec mauvaise perfusion nécessite un début de réanimation (RCP) selon les recommandations PALS.
Causes : Hypoxie (cause n°1), vagotonie sévère, hypertension intracrânienne (triade de Cushing), hypothermie, hypothyroïdie, intoxications (bêta-bloquants, inhibiteurs calciques, digoxine).
Battements supraventriculaires et ventriculaires prématurés
Extrasystoles supraventriculaires (ESSV) : Très fréquentes chez le nouveau-né, souvent bénignes et disparaissant dans les premiers mois. Si elles sont très nombreuses, elles peuvent (rarement) induire une tachycardie incessante.
Extrasystoles ventriculaires (ESV) : Présentes chez jusqu’à 20-30% des enfants sains sur un Holter de 24h. Critères de bénignité : monomorphes, isolées, disparaissant à l’effort, cœur structurellement normal. Des ESV polymorphes, en doublets/salves, ou s’aggravant à l’effort nécessitent une exploration approfondie (échocardiographie, épreuve d’effort, IRM cardiaque) pour exclure une cardiomyopathie ou une canalopathie (CPVT).
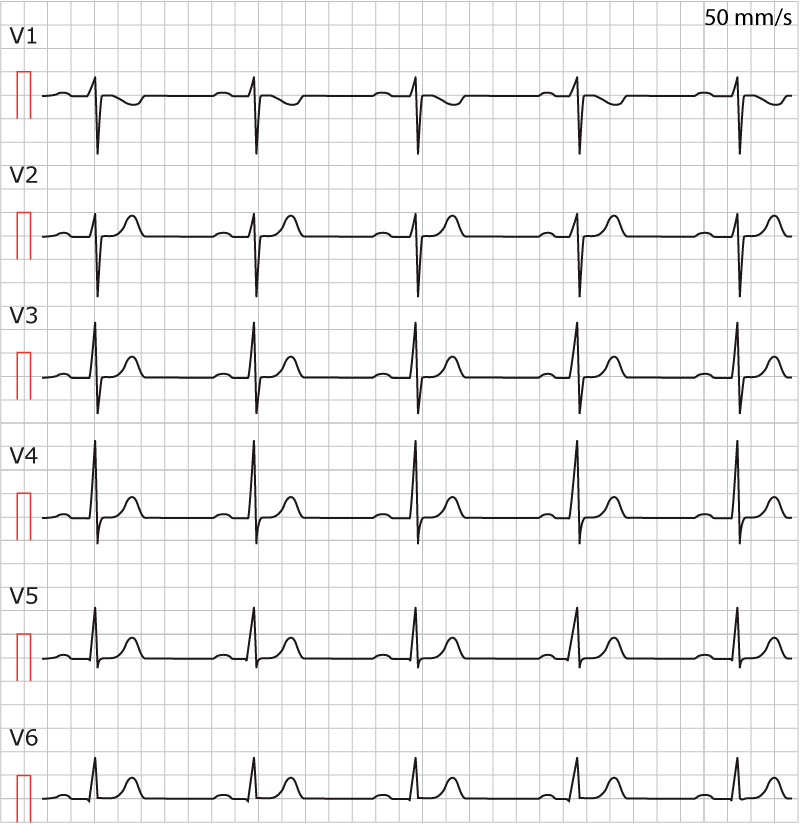
Onde P et hypertrophies auriculaires
L’onde P représente la dépolarisation auriculaire.
Valeurs normales : Amplitude < 2,5 mm (ou 0,25 mV) et durée < 0,08 s chez le nourrisson / < 0,10 s chez l'enfant.
Anomalies auriculaires
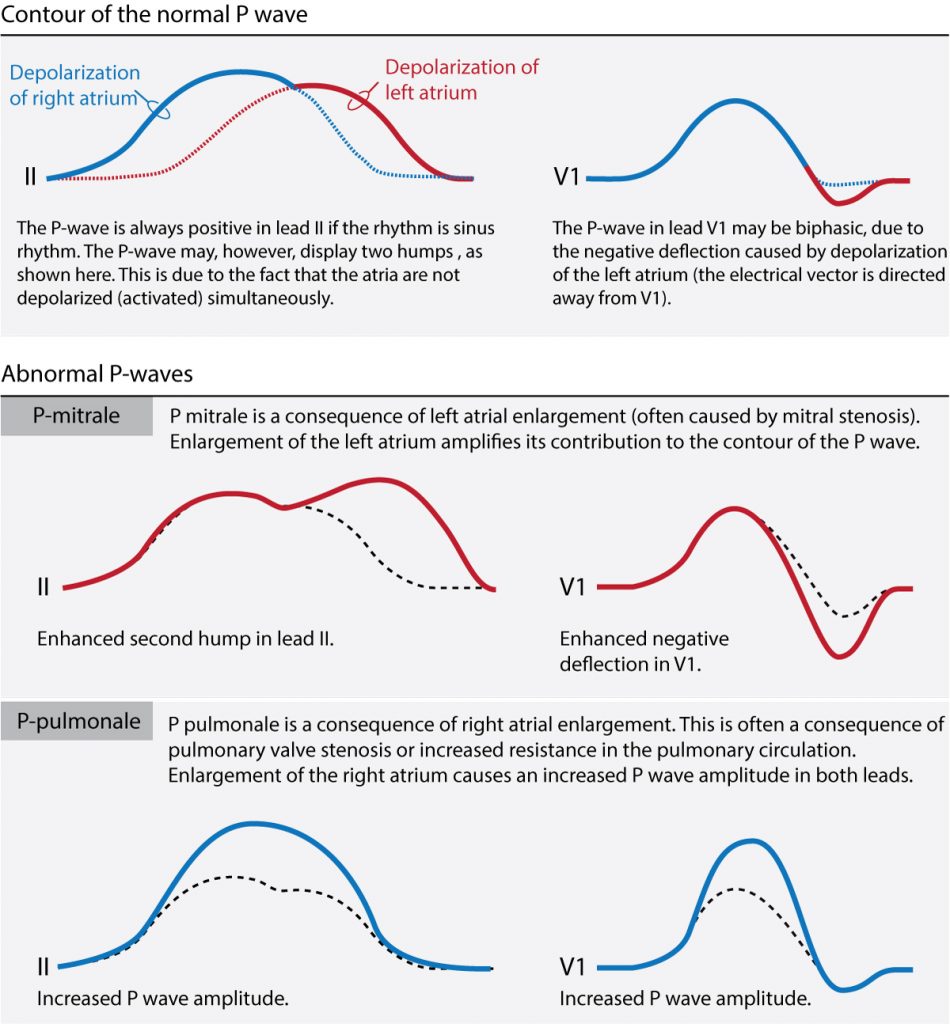
Hypertrophie auriculaire droite (P pulmonaire)
Ondes P hautes et pointues (« en pic ») en DII, DIII, aVF (> 2,5 mm). Fréquent dans les cardiopathies avec obstacle droit (atrésie tricuspide, sténose pulmonaire sévère, tétralogie de Fallot) ou hypertension pulmonaire.
Hypertrophie auriculaire gauche (P mitrale)
Ondes P larges et bifides (« en M ») en DII (durée > 0,10 s ou > 0,12 s selon l’âge) et composante négative terminale profonde et large en V1. Observé dans les shunts gauche-droite importants (PCA, CIV large) ou les obstacles mitraux/aortiques.
4. Intervalle PR
L’intervalle PR varie avec la fréquence cardiaque et l’âge. Il est plus court chez le nourrisson (min 80-90 ms) et s’allonge avec la croissance.
Pré-excitation et bloc auriculo-ventriculaire (AV)
Un intervalle PR court (< 90 ms chez le nourrisson, < 120 ms chez l'enfant plus grand) suggère une pré-excitation (WPW) ou une maladie de surcharge (Pompe, Fabry). Voir section Pré-excitation et syndrome de Wolff-Parkinson-White.
Un intervalle PR prolongé définit le bloc AV.
Bloc AV du 1er degré : Allongement fixe du PR au-delà de la norme pour l’âge. Fréquent dans les CIA (communication interauriculaire), l’anomalie d’Ebstein, le RAA (Rhumatisme Articulaire Aigu), ou sous digoxine.
Bloc AV du 2ème degré : Le type 1 (Wenckebach) peut être physiologique durant le sommeil chez l’enfant sportif. Le type 2 est pathologique.
Bloc AV du 3ème degré (complet) :
Congénital : Associé au lupus maternel (anticorps anti-SSA/Ro et anti-SSB/La traversant le placenta et lésant le tissu de conduction fœtal) ou à des cardiopathies complexes (transposition corrigée des gros vaisseaux).
Acquis : Post-chirurgical (réparation de CIV, Tetralogie de Fallot) ou infectieux (Lyme, myocardite virale, diphtérie).
Diagnostics différentiels d’un PR court
- Pré-excitation (WPW)
- Maladie de Pompe (Glycogénose type II) : associe PR court et QRS géants (HVG massive).
- Rythme auriculaire bas (foyer proche du nœud AV).
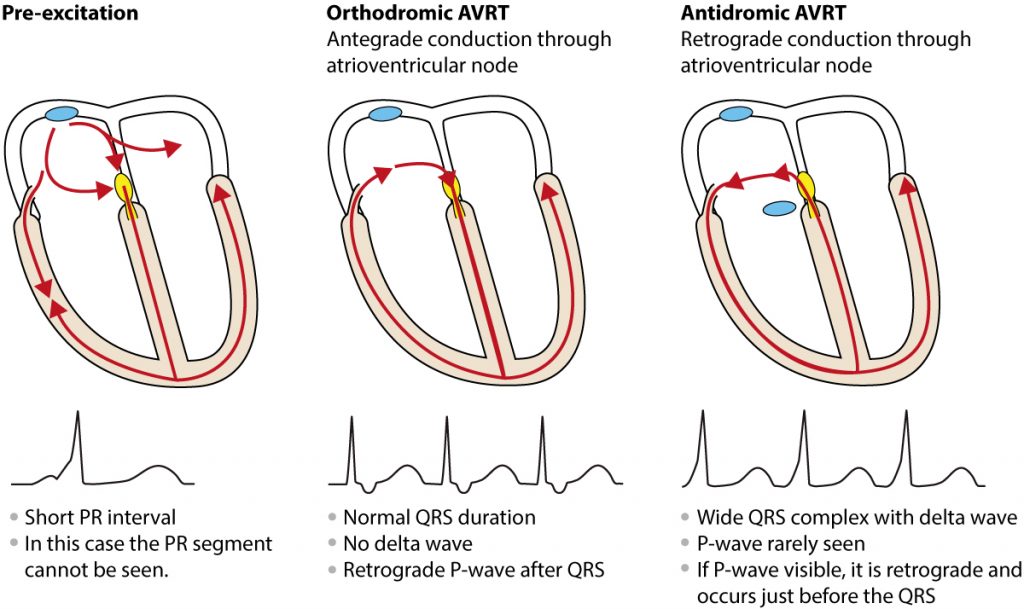
Voies accessoires et pré-excitation (WPW)
Le syndrome de Wolff-Parkinson-White est l’une des causes les plus fréquentes de tachycardie chez l’enfant. Il résulte d’un faisceau de conduction accessoire (faisceau de Kent) contournant le filtre du nœud AV.
Caractéristiques cliniques et ECG
Chez le nourrisson, la conduction par la voie accessoire peut être rapide et dangereuse. Cependant, une proportion significative de voies accessoires présentes à la naissance perdent leur capacité de conduction antérograde au cours de la première année de vie (« guérison » spontanée apparente).
La triade ECG classique associe : PR court + Onde Delta + QRS large.
Attention : Chez le nouveau-né, l’intervalle PR étant physiologiquement court, la pré-excitation peut être difficile à discerner.
Alerte de sécurité : En cas de fibrillation auriculaire pré-excitée (rare chez l’enfant mais possible chez l’adolescent), l’adénosine, les bêta-bloquants, les inhibiteurs calciques et la digoxine sont contre-indiqués car ils peuvent favoriser une conduction ultra-rapide par la voie accessoire vers le ventricule, entraînant une fibrillation ventriculaire.
Le complexe QRS : Évolution physiologique et pathologique
Axe électrique et Dominance Ventriculaire
C’est la notion la plus importante en ECG pédiatrique.
À la naissance et chez le nouveau-né : Le ventricule droit (VD) est prédominant (plus épais et plus musclé que le gauche) car il a assuré l’essentiel du débit combiné fœtal contre des résistances pulmonaires élevées. L’axe du QRS est donc dévié à droite (entre +90° et +180°). Les ondes R sont grandes en V1-V2.
Évolution : Avec la chute des résistances pulmonaires, le ventricule gauche (VG) se développe. L’axe se normalise progressivement vers la gauche.
Enfant et adolescent : L’axe devient adulte (entre -30° et +90°). Une déviation axiale droite persistante (ex: axe > 90° après 3-4 ans) est pathologique et suggère une hypertrophie ventriculaire droite (HVD) ou un hémibloc postérieur gauche.
Durée du QRS
La durée du QRS est plus courte chez l’enfant en raison de la petite taille du cœur.
Nouveau-né : < 80 ms.
Enfant : < 90 ms.
Adolescent : < 100-110 ms.
Un QRS de 100 ms peut être normal chez un adulte mais indiquer un retard de conduction intraventriculaire significatif chez un nourrisson.
Morphologie R/S et progression
Nouveau-né : Rapport R/S > 1 en V1 (Dominance droite). Pas d’onde Q en V1.
Après 3-5 ans : Le rapport R/S en V1 devient < 1 (Dominance gauche s'installant).
Une onde R exclusive en V1 (sans onde S) ou un aspect qR en V1 sont toujours pathologiques et signent une HVD sévère.
Ondes Q pathologiques
- Ondes Q profondes et étroites : Peuvent être normales en dérivations inférieures et V5-V6 (Q septales physiologiques, reflet de l’hypertrophie septale relative).
- Ondes Q larges (> 30 ms) ou profondes (> 4-5 mm) : Suggèrent une hypertrophie ventriculaire (HVD si en V1, HVG si en V6) ou une ischémie.
- Complexe QR en V1 : Pathognomonique de l’HVD.
- Ondes Q profondes en I, aVL : Anomalie de naissance de la coronaire gauche (ALCAPA) à suspecter chez un nourrisson algique/insipide.
Hypertrophie ventriculaire droite (HVD)
En raison de la dominance droite physiologique initiale, le diagnostic d’HVD est subtil. Signes évocateurs :
- Onde R pure en V1 (> 10-15 mm selon l’âge) ou aspect qR en V1.
- Onde T positive en V1 après J7 de vie (signe très spécifique avant 10 ans).
- Axe QRS hyper-droit pour l’âge.
- Ondes S profondes en V6.
- Aspect rSR’ en V1 avec R’ > 10-15 mm.
Hypertrophie ventriculaire gauche (HVG)
Moins fréquente chez le nourrisson, elle se voit dans les obstacles gauches (sténose aortique, coarctation) ou les myocardiopathies.
Critères de voltage (indices de Sokolow-Lyon souvent peu adaptés, préférer les percentiles) : Ondes R très amples en V5-V6 et S profondes en V1.
Signes de surcharge (strain) : Dépressions ST et inversion T en V5-V6.
Cardiomyopathie hypertrophique (CMH)
La CMH est la première cause de mort subite chez le jeune athlète. L’ECG est anormal dans > 90% des cas.
Signes d’appel :
– Voltages QRS pseudo-normaux ou très augmentés.
– Ondes Q de pseudo-nécrose profondes et fines en latéral (I, aVL, V5, V6) ou inférieur, reflétant l’hypertrophie septale.
– Troubles de la repolarisation diffus.
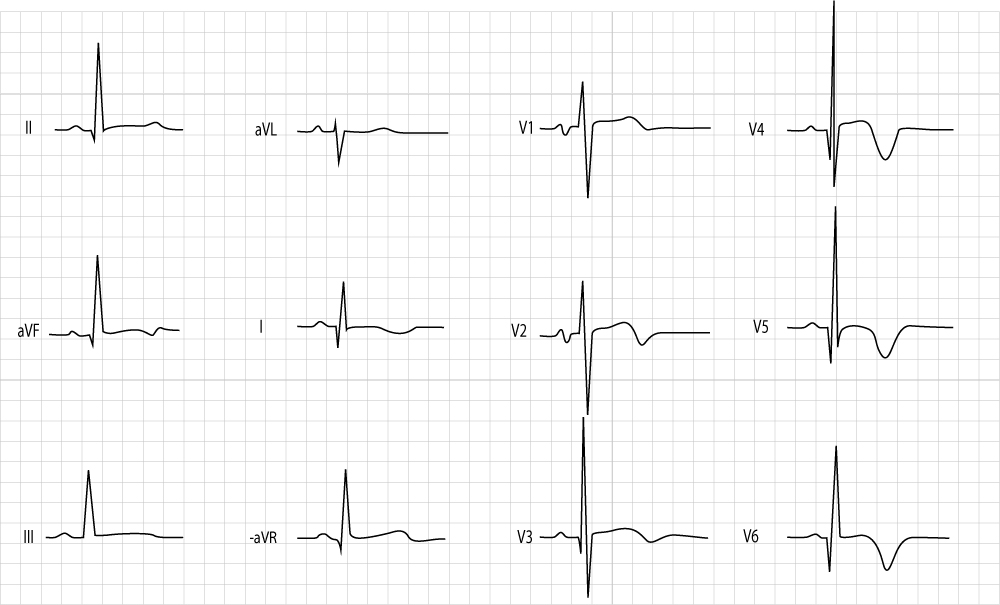
Le segment ST et l’onde T : Particularités pédiatriques
Repolarisation précoce : Un sus-décalage du point J concave vers le haut est très fréquent chez l’adolescent sain (surtout masculin), mimant parfois une péricardite ou un syndrome de Brugada (mais l’aspect en « selle de cheval » ou le dôme sont absents dans la repolarisation précoce bénigne).
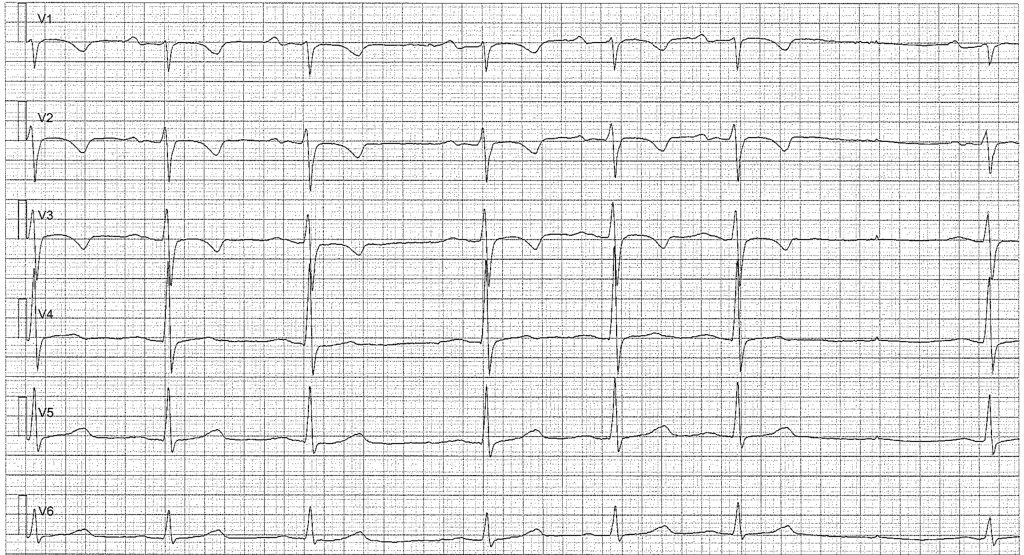
Syndrome de la T-négative juvénile :
C’est une variante normale fondamentale à reconnaître.
– À la naissance : T positive en V1.
– De J7 à l’adolescence : L’onde T devient négative en V1, V2, V3 (et parfois V4). C’est le pattern juvénile normal.
– Pathologique : Une onde T positive en V1 chez un enfant de 5 ans est anormale et suggère une HVD.
– À la puberté : L’onde T se positive progressivement de V4 vers V1. La persistance d’une onde T négative en V1-V2 chez la femme adulte est fréquente et bénigne.
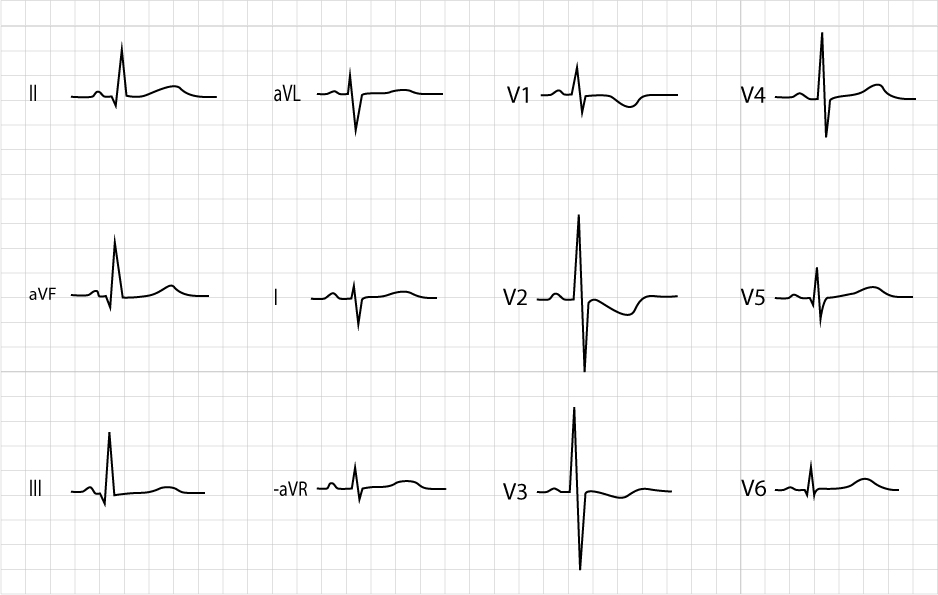
Intervalle QT (QTc)
Le syndrome du QT long (SQTL) congénital est une canalopathie potentiellement létale (torsades de pointes). Le dépistage néonatal est parfois proposé mais débattu.
Mesure : Le calcul manuel est indispensable, surtout en cas d’arythmie sinusale marquée. Utiliser la formule de Bazett, bien qu’elle surestime le QTc à fréquences élevées (fréquentes chez le nourrisson).
Valeurs seuils :
– QTc normal : < 440 ms (hommes), < 460 ms (femmes/enfants).
– QTc limite (zone grise) : 440-460 ms.
– QTc allongé pathologique : > 470 ms (ou > 460 ms répété).
– Risque majeur : > 500 ms.

L’hypocalcémie est une cause classique d’allongement du QT (segment ST long) chez le nouveau-né (syndrome de DiGeorge ou hypoparathyroïdie).
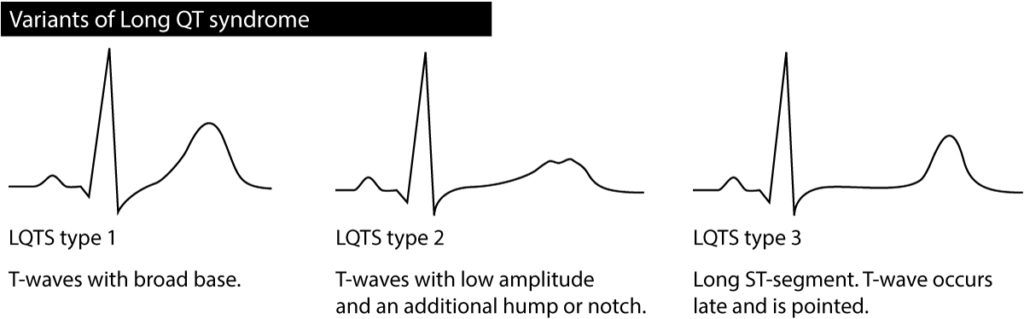
Syndrome du QT court
Rare mais très arythmogène (FA, FV). Défini par un QTc < 330-340 ms. Attention à ne pas confondre avec l'effet de la digoxine ou l'hypercalcémie.