Introduction à la maladie coronarienne (cardiopathie ischémique)
Coronaropathie (cardiopathie ischémique)
- L’athérosclérose : physiopathologie de la maladie coronarienne
- Angine de poitrine : présentation clinique et classification
- Syndrome coronarien aigu et infarctus du myocarde
- Facteurs de risque de la maladie coronarienne
- L’ECG dans les cardiopathies ischémiques
- Au-delà de l’ECG : Diagnostic biologique et imagerie
- Le scénario de la tempête parfaite : chronobiologie et instabilité
- Principes généraux de la prise en charge
- Références
La maladie coronarienne, synonyme de cardiopathie ischémique, représente la forme la plus prévalente de maladie cardiovasculaire et demeure un défi majeur de santé publique. Depuis plus d’un demi-siècle, elle constitue la première cause de mortalité dans les pays occidentaux et les pays à revenu élevé, où elle est responsable d’environ 20 % de l’ensemble des décès. Bien que les taux de mortalité et de létalité de la maladie coronarienne aient atteint leur apogée dans les années 1970 pour diminuer ensuite de manière constante, le fardeau absolu de la maladie reste élevé en raison du vieillissement de la population.
Ce déclin marqué des taux de mortalité standardisés par l’âge s’explique par le succès des stratégies de prévention primaire et secondaire, notamment la réduction du tabagisme, le contrôle strict de l’hypertension artérielle et l’abaissement agressif des lipides sanguins par les statines et, plus récemment, les inhibiteurs de PCSK9. Parallèlement, l’avènement des unités de soins intensifs coronariens et de la revascularisation précoce a transformé le pronostic aigu. Toutefois, la maladie coronarienne reste la première cause de mortalité dans la plupart des régions du monde et la morbidité associée (insuffisance cardiaque ischémique) continue de croître (Tsao et al.).
The New England Journal of Medicine, 1812. Remarques sur l’angine de poitrine par John Warren
Les faits remarquables, à savoir que le paroxysme, voire la maladie elle-même, est plus particulièrement déclenché en montant une colline et après un repas ; qu’ainsi déclenché, il s’accompagne d’une sensation qui menace de mort instantanée si le mouvement est poursuivi ; et qu’en s’arrêtant, la détresse s’atténue immédiatement ou disparaît complètement, ont constitué une partie constitutive du caractère de l’angine de poitrine.
L’athérosclérose : physiopathologie de la maladie coronarienne
L’étiologie fondamentale de la maladie coronarienne est l’athérosclérose, une pathologie inflammatoire chronique et progressive de l’intima des artères. Au cours des dernières décennies, la compréhension physiopathologique a évolué : l’athérosclérose n’est plus considérée comme un simple dépôt passif de lipides, mais comme une réponse immunitaire et inflammatoire active à une agression endothéliale. Le processus débute souvent par une dysfonction endothéliale, favorisée par des contraintes de cisaillement (shear stress) et des facteurs de risque cardiovasculaire, permettant la pénétration des lipoprotéines de basse densité (LDL) dans l’espace sous-intimal.
Une fois oxydées, ces particules LDL stimulent le recrutement de monocytes qui se différencient en macrophages. Ces derniers phagocytent les lipides oxydés pour devenir des cellules spumeuses (foam cells), initiant la formation de la strie lipidique. Au fur et à mesure que l’inflammation et le dépôt de lipides progressent, une plaque d’athérosclérose complexe se structure, composée d’un cœur nécrotique riche en lipides et débris cellulaires, recouvert d’une chape fibreuse plus ou moins épaisse. Ces plaques commencent à se former dès l’enfance. L’interaction entre l’inflammation systémique et locale et les facteurs de risque (tabagisme, hypertension, dyslipidémie, diabète) dicte la vitesse de progression de la plaque et sa vulnérabilité. Plus l’inflammation est intense (marquée par exemple par une CRP-us élevée), plus la plaque est susceptible de se déstabiliser, menant aux événements aigus (Stone, Libby et al.).
Sur le plan hémodynamique, à mesure que la plaque d’athérome croît, elle fait saillie dans la lumière artérielle, provoquant une sténose. Cette réduction du calibre artériel limite la réserve coronaire. Au repos, le débit peut rester suffisant, mais lors d’une augmentation de la demande myocardique en oxygène (MVO2) — typiquement à l’effort — le flux sanguin ne peut augmenter adéquatement. Lorsque la demande en oxygène dépasse l’apport, une ischémie tissulaire survient, se manifestant cliniquement par l’angine de poitrine. Ce déséquilibre entre l’offre et la demande est le mécanisme central de l’angor stable.
Angine de poitrine : présentation clinique et classification
L’angine de poitrine (angor) est le symptôme cardinal de l’ischémie myocardique. Elle est typiquement décrite comme une douleur rétrosternale diffuse, constrictive (« en étau »), ou une sensation de lourdeur, de brûlure ou d’oppression. L’irradiation classique se fait vers l’épaule et le bras gauches, le cou, la mâchoire inférieure ou le dos. L’angine de poitrine s’accompagne souvent de symptômes neurovégétatifs ou d’une dyspnée d’effort (équivalent angineux).
Dans la forme stable, les symptômes sont prévisibles et reproductibles pour un même niveau d’effort. Le patient ne ressent de douleur que lorsque la consommation myocardique en oxygène (MVO2) augmente (exercice, émotion forte, digestion, froid), et le soulagement est obtenu rapidement (en moins de 5 minutes) par l’arrêt de l’effort ou la prise de trinitrine sublinguale (test diagnostic et thérapeutique).
Classification de la Société Canadienne de Cardiologie (CCS)
Pour standardiser l’évaluation de la sévérité de l’angor stable, la classification CCS est universellement utilisée :
- Classe I : L’activité physique ordinaire (marcher, monter des escaliers) ne provoque pas d’angine. L’angine survient lors d’efforts intenses, rapides ou prolongés.
- Classe II : Légère limitation de l’activité ordinaire. L’angine survient à la marche rapide, en montée, après les repas, ou par temps froid.
- Classe III : Limitation marquée de l’activité physique ordinaire. L’angine survient en marchant un ou deux pâtés de maisons sur le plat ou en montant un étage à vitesse normale.
- Classe IV : Incapacité à mener une activité physique sans inconfort ; l’angine peut être présente au repos.
Il est crucial de noter que la présentation clinique peut être atypique, particulièrement chez les femmes, les personnes âgées et les diabétiques. Chez ces patients, la douleur thoracique peut être absente, remplacée par une dyspnée isolée, une fatigue extrême, des nausées ou des douleurs épigastriques. On parle alors d’équivalents angineux.
La taille des plaques coronaires a tendance à augmenter avec le temps, aggravant la sténose et les symptômes. Cependant, des recherches majeures (étude JUPITER, REVERSAL, GLAGOV) ont démontré qu’un traitement hypolipémiant intensif (statines à forte dose, ézétimibe, inhibiteurs PCSK9) permet non seulement de stabiliser la plaque, mais parfois d’obtenir une régression du volume de l’athérome.
De la plaque stable à la rupture : physiopathologie des syndromes coronariens aigus
Le basculement vers la pathologie aiguë survient lorsque la plaque d’athérome subit une modification structurelle soudaine : soit une rupture de la chape fibreuse, soit une érosion endothéliale. Ce phénomène est intimement lié à l’activité inflammatoire au sein de la plaque (abondance de macrophages sécrétant des métalloprotéases qui dégradent le collagène de la chape fibreuse).
Une plaque rompue expose le cœur lipidique hautement thrombogène (facteur tissulaire) au flux sanguin. S’ensuit une activation plaquettaire immédiate et le déclenchement de la cascade de coagulation, aboutissant à la formation d’un thrombus (athérothrombose). Si le thrombus est occlusif, il interrompt totalement le flux sanguin, provoquant une ischémie transmurale sévère (généralement associée à un sus-décalage du segment ST). Si le thrombus est sub-occlusif ou transitoire, l’ischémie est moins profonde mais tout aussi dangereuse. Ce spectre clinique constitue le syndrome coronarien aigu (SCA). Contrairement à l’angor stable, la douleur du SCA survient souvent au repos, est plus intense, dure plus longtemps (> 20 minutes) et résiste à la trinitrine (voir Figure 1).
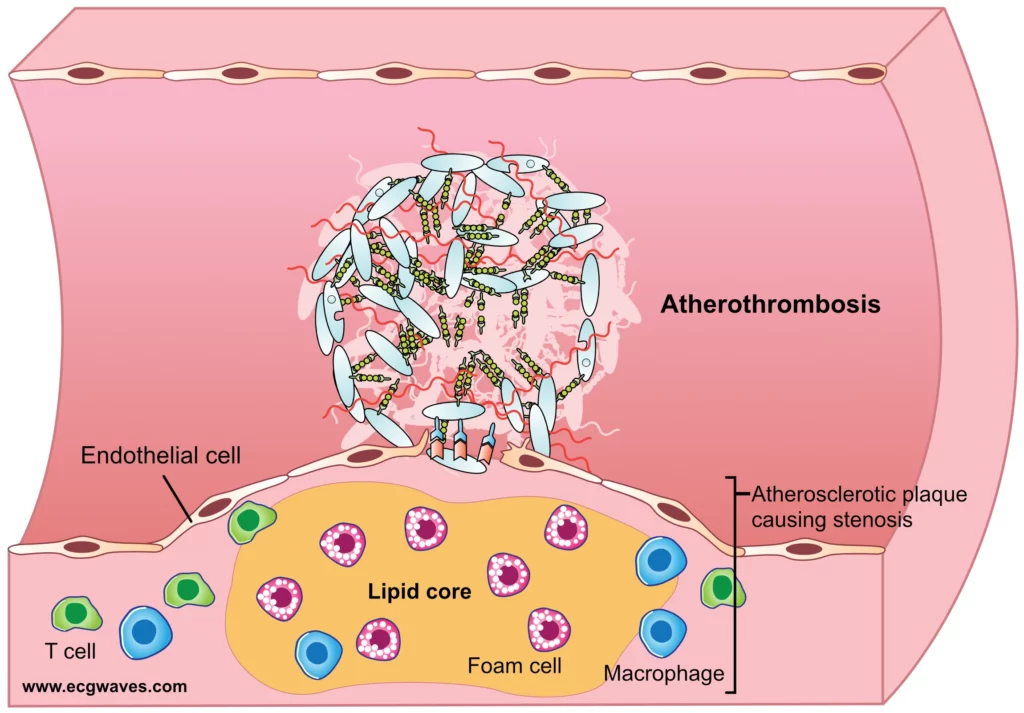
Syndrome coronarien aigu et infarctus du myocarde
Le syndrome coronarien aigu représente une urgence vitale. L’interruption du flux sanguin déclenche une cascade d’événements : hypoxie cellulaire, arrêt de la contraction (akinésie) en quelques secondes, et début de la nécrose cellulaire (infarctus) en 20 à 40 minutes. C’est le concept de « Time is Muscle ».
L’infarctus progresse du sous-endocarde (couche la plus sensible à l’ischémie) vers le sous-épicarde (front de vague de la nécrose). Si l’artère est complètement occluse et non revascularisée, la nécrose devient transmurale en 6 à 12 heures, entraînant une perte définitive de fonction contractile. Les complications immédiates incluent les arythmies ventriculaires malignes (fibrillation ventriculaire), cause principale de mort subite pré-hospitalière, et le choc cardiogénique. À long terme, la perte de myocarde conduit au remodelage ventriculaire et à l’insuffisance cardiaque chronique.
Il convient de noter que l’évolution naturelle est hétérogène. Certains patients développent une circulation collatérale protectrice qui peut limiter l’étendue de l’infarctus même en cas d’occlusion complète. D’autre part, la définition universelle de l’infarctus du myocarde distingue l’infarctus de Type 1 (rupture de plaque/thrombose, le mécanisme classique décrit ici) de l’infarctus de Type 2 (déséquilibre offre/demande sans événement thrombotique aigu, par exemple lors d’une anémie sévère, d’une tachyarythmie ou d’un choc septique). Cette distinction est fondamentale car le traitement diffère radicalement.
Facteurs de risque de la maladie coronarienne
L’identification et le contrôle des facteurs de risque constituent la pierre angulaire de la prévention cardiovasculaire. L’étude INTERHEART, étude cas-témoins historique menée dans 52 pays, a révolutionné notre compréhension en démontrant que plus de 90 % du risque attribuable de développer un premier infarctus du myocarde est expliqué par neuf facteurs de risque modifiables. Ce constat est universel, s’appliquant aux deux sexes et à toutes les régions géographiques.
Facteurs de risque traditionnels et émergents
Les facteurs les plus puissants sont l’apoB/apoA1 ratio (reflet de la dyslipidémie athérogène) et le tabagisme. Cependant, la médecine cardiovasculaire moderne s’intéresse également aux facteurs de risque dits « non traditionnels » ou émergents, tels que la Lipoprotéine(a) [Lp(a)], une particule génétiquement déterminée et hautement athérogène, ainsi que l’inflammation chronique de bas grade (mesurée par la CRP ultra-sensible).
Tableau 1 : Facteurs de risque d’infarctus aigu du myocarde (étude INTERHEART)
| FACTEUR DE RISQUE | RISQUE RELATIF (Odds Ratio) |
| Dyslipidémie (Ratio ApoB/ApoA1 élevé) | 3,25 |
| Tabagisme actuel | 2,87 |
| Diabète | 2,37 |
| Hypertension artérielle | 1,91 |
| Obésité abdominale (Rapport Taille/Hanche) | 1,62 |
| Stress psychosocial | 2,67 |
| Consommation quotidienne de légumes et de fruits | 0,70 (Facteur protecteur) |
| Exercice physique régulier | 0,86 (Facteur protecteur) |
| Consommation modérée d’alcool | 0,91 (Facteur protecteur) |
Interprétation clinique : L’hyperlipidémie (dyslipidémie) est le facteur prédictif le plus puissant au niveau de la population (OR 3,25). Le « mauvais cholestérol » (LDL-c) est le moteur principal de l’athérosclérose ; le consensus actuel établit que « plus c’est bas, mieux c’est » (the lower, the better) pour les patients à risque. Le tabagisme présente un effet dose-dépendant mais sans seuil de sécurité : même une consommation minime (1-5 cigarettes/jour) augmente le risque de 40 %. L’obésité abdominale (adiposité viscérale) est un marqueur métabolique plus pertinent que l’IMC global pour prédire le risque coronarien.
L’ECG dans les cardiopathies ischémiques
L’électrocardiogramme (ECG) à 12 dérivations reste l’outil diagnostique de première ligne, indispensable pour la stratification du risque et la décision thérapeutique immédiate. Son interprétation repose sur la corrélation entre les modifications électriques et la physiologie cellulaire.
L’ischémie aiguë perturbe principalement la repolarisation ventriculaire. Les cellules ischémiques, manquant d’ATP, ne peuvent maintenir les gradients ioniques transmembranaires, ce qui crée des courants de lésion. Cela se traduit par des modifications du segment ST et de l’onde T :
- Ischémie sous-endocardique : Se manifeste généralement par des ondes T amples et pointues ou un sous-décalage du segment ST.
- Ischémie sous-épicardique (ou transmurale) : Se manifeste classiquement par un sus-décalage du segment ST (onde de Pardee) dans les dérivations faisant face à la zone ischémique.
L’infarctus constitué (nécrose) affecte la dépolarisation. Le tissu nécrosé étant électriquement inerte, il agit comme une « fenêtre » électrique, modifiant le vecteur QRS. La séquelle classique est l’apparition d’ondes Q pathologiques (durée > 0,04s, amplitude > 25% de l’onde R) et la perte d’amplitude de l’onde R (rabotage).
Classification ECG des syndromes coronariens
La distinction fondamentale basée sur l’ECG réalisé dans les 10 premières minutes de la prise en charge (Premier Contact Médical) dicte la stratégie de reperfusion :
- Maladie coronarienne stable : L’ECG de repos est souvent strictement normal (environ 50% des cas) ou montre des séquelles d’infarctus anciens. L’ischémie doit être provoquée par une épreuve d’effort (ECG d’effort) ou une imagerie de stress pour être détectée (sous-décalage ST horizontal ou descendant).
- Syndromes Coronariens Aigus (SCA) :
- SCA avec sus-décalage du segment ST (STEMI) : Présence d’un sus-décalage persistant (> 20 min) du segment ST dans au moins deux dérivations contiguës. Cela signe généralement une occlusion coronaire totale aiguë. La stratégie est la reperfusion immédiate (angioplastie primaire ou thrombolyse).
- SCA sans sus-décalage du segment ST (NSTE-ACS) : L’ECG peut montrer un sous-décalage du segment ST, une inversion des ondes T, ou être normal. L’artère est souvent sub-occluse ou l’occlusion est intermittente. Le diagnostic différentiel entre NSTEMI (avec nécrose, troponines positives) et Angor Instable (sans nécrose, troponines négatives) se fait par la biologie.
Au-delà de l’ECG : Diagnostic biologique et imagerie
Bien que l’ECG soit central, le diagnostic moderne de la coronaropathie s’appuie sur une approche multimodale.
Le rôle central des Troponines (hs-cTn)
Les troponines cardiaques (I ou T) sont des protéines structurelles du cardiomyocyte. Leur détection dans le sang est le signe le plus sensible et spécifique de lésion myocardique. Les dosages de troponine haute sensibilité (hs-cTn) permettent aujourd’hui de détecter des micro-nécroses très précocement. Dans le cadre d’un SCA, on recherche une cinétique (élévation ou décroissance) des taux de troponine pour confirmer le diagnostic d’infarctus aigu (NSTEMI).
Imagerie Cardiaque non invasive
Avant la coronarographie invasive, l’imagerie joue un rôle croissant :
- Échocardiographie de repos : Recherche des troubles de la cinétique segmentaire (une zone qui ne se contracte pas suggère une ischémie ou un infarctus) et évalue la fonction ventriculaire gauche (FEVG).
- Coroscanner (Angio-TDM coronaire) : Cet examen anatomique permet de visualiser directement les artères coronaires. Il a une excellente valeur prédictive négative pour exclure la maladie coronarienne chez les patients à risque faible ou intermédiaire.
Le scénario de la tempête parfaite : chronobiologie et instabilité
L’incidence annuelle des SCA est relativement faible par rapport à la prévalence de l’athérosclérose, ce qui suggère que la rupture de plaque est nécessaire mais non suffisante pour provoquer un événement clinique. Des études autopsiques montrent que de nombreuses ruptures de plaque sont asymptomatiques et cicatrisent silencieusement, contribuant à la progression par paliers de la sténose.
Le concept de « tempête parfaite » postule que le SCA survient lorsque la rupture de plaque coïncide avec un état pro-thrombotique systémique transitoire (« sang vulnérable »). Il existe une variation circadienne marquée : l’incidence des infarctus et de la mort subite est maximale le matin (entre 6h et midi). Cela correspond au pic physiologique de catécholamines, d’agrégabilité plaquettaire, de viscosité sanguine et de tonus vasculaire au réveil.
L’imagerie endocoronaire (IVUS – échographie intravasculaire, et OCT – tomographie par cohérence optique) a permis de caractériser la « plaque vulnérable » : elle possède typiquement une chape fibreuse fine (< 65 µm) et un gros cœur lipidique. Cependant, la prédiction des événements reste complexe car la morphologie des plaques est dynamique. Sous traitement statine intensif, la chape fibreuse peut s'épaissir et le cœur lipidique diminuer, stabilisant ainsi la plaque (phénomène de passivation). Le risque thrombotique est donc modifiable.
Contrairement à une idée reçue, les infarctus les plus sévères surviennent souvent sur des plaques qui n’étaient pas sévèrement sténosantes avant la rupture (< 50-70% de sténose). Ces plaques, moins calcifiées et plus riches en lipides, sont mécaniquement plus fragiles et n'ont pas permis le développement d'une circulation collatérale, d'où l'importance de traiter l'athérosclérose systémique et non seulement les sténoses visibles.
Principes généraux de la prise en charge
Le traitement de la maladie coronarienne repose sur trois piliers complémentaires :
- Le traitement médical optimal : Il vise à réduire la consommation d’oxygène (bêta-bloquants, inhibiteurs calciques), prévenir la thrombose (antiagrégants plaquettaires comme l’aspirine et le clopidogrel/ticagrelor) et stabiliser l’athérosclérose (statines haute intensité, IEC).
- La revascularisation myocardique : Elle peut être percutanée (Angioplastie par ballonnet avec pose de stent) ou chirurgicale (Pontage aorto-coronarien – PAC). Le choix dépend de la complexité anatomique des lésions (Score SYNTAX) et du terrain du patient (diabète, fonction cardiaque).
- La modification du mode de vie : L’arrêt du tabac, l’alimentation méditerranéenne, l’activité physique régulière et la gestion du stress sont aussi efficaces que les médicaments pour prévenir les récidives.
Références
Arbab-Zadeh et al. : Acute Coronary Events ; Circulation 2012
Tsao CW, Aday AW, Almarzooq ZI, et al. Heart Disease and Stroke Statistics-2022 Update : A Report From the American Heart Association. Circulation 2022 ; 145: e153-639.
Stone PH, Libby P, Boden WE. Fundamental Pathobiology of Coronary Atherosclerosis and Clinical Implications for Chronic Ischemic Heart Disease Management-The Plaque Hypothesis : A Narrative Review, JAMA Cardiol 2023 ; 8: 192.
Yusuf S, Hawken S, Ounpuu S, et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet 2004; 364: 937–52.
Thygesen K, Alpert JS, Jaffe AS, et al. Fourth Universal Definition of Myocardial Infarction (2018). Circulation 2018; 138:e618-e651.