Bloc de branche gauche (BBG) dans l’infarctus aigu du myocarde : les critères de Sgarbossa
Bloc de branche gauche (BBG) dans l’infarctus aigu du myocarde (IAM) : implications cliniques et critères de Sgarbossa
Contrairement au bloc de branche droit (BBD), le bloc de branche gauche (BBG) est presque toujours un résultat pathologique témoignant d’une atteinte myocardique sous-jacente qui affecte significativement la mortalité cardiovasculaire et totale. Le bloc de branche gauche est plus fréquent chez les patients souffrant d’une cardiopathie structurelle avancée, d’hypertension de longue date et de cardiopathie ischémique. L’évaluation de l’ischémie sur l’ECG est notoirement difficile en présence d’un BBG. En effet, l’activation ventriculaire anormale (de droite à gauche) propre au BBG entraîne des modifications substantielles de la dépolarisation et, par conséquent, de la repolarisation du ventricule gauche. Ces altérations se traduisent par des modifications secondaires du segment ST-T qui sont physiologiques dans ce contexte, obéissant au principe de discordance appropriée (le segment ST et l’onde T s’opposent à la direction principale du complexe QRS). Ces modifications du segment ST-T peuvent imiter (simuler) ou masquer une ischémie, rendant le diagnostic d’infarctus particulièrement complexe.
La simulation de l’ischémie se manifeste par des élévations du segment ST (sus-décalages) dans les dérivations précordiales droites (V1 à V3), souvent accompagnées de dépressions du segment ST (sous-décalages) dans les dérivations latérales (V5, V6, I et aVL). Les cliniciens confondent souvent ces élévations et dépressions, qui sont secondaires à la repolarisation anormale, avec celles causées par un infarctus aigu du myocarde avec sus-décalage du segment ST (STEMI). En effet, plusieurs études épidémiologiques et registres de cathétérisme ont montré que la majorité des patients adressés à tort au laboratoire de cathétérisme (fausses alertes) avec une suspicion de STEMI présentent un bloc de branche gauche (BBG) chronique sans occlusion coronaire aiguë.
Le masquage de l’ischémie se produit parce que les changements ST-T induits par le BBG (la discordance appropriée) sont souvent de plus grande amplitude que les courants de lésion causés par l’ischémie. Par conséquent, les modifications ischémiques (vecteurs de lésion) sont annulées ou masquées par les vecteurs de repolarisation du bloc et ne deviennent pas apparentes sur le tracé de surface. Il existe toutefois des exceptions à cette règle, notamment lorsque l’ischémie provoque une modification vectorielle qui va dans le même sens que la repolarisation anormale ou l’exagère de manière disproportionnée. Pour relever ces défis, les chercheurs ont développé des critères ECG spécifiques conçus pour identifier l’ischémie en présence d’un BBG. Les critères les plus largement reconnus et validés à ce jour ont été mis au point par Elena Sgarbossa et ses collègues en 1996, issus de la sous-analyse de l’étude GUSTO-1, et sont donc appelés « critères de Sgarbossa ». Cependant, bien que très spécifiques, les critères originaux manquent de sensibilité. Le jugement clinique, intégrant l’histoire du patient et l’instabilité hémodynamique, reste un outil indispensable et plus fiable pour évaluer l’ischémie dans ces cas, un point souligné avec force dans les directives internationales récentes.
Implications du bloc de branche gauche dans l’ischémie et l’infarctus du myocarde
Le diagnostic différentiel face à un BBG chez un patient douloureux est un défi quotidien. Voici un résumé approfondi des problématiques cliniques lorsqu’un patient présente un bloc de branche gauche (BBG) et des symptômes évocateurs d’ischémie :
- Le bloc de branche gauche (BBG) peut imiter l’infarctus aigu du myocarde avec sus-décalage du segment ST (STEMI) : Il se présente souvent avec des modifications similaires de l’ECG, notamment des élévations du segment ST concaves vers le haut en antéro-septal, des dépressions du segment ST en latéral, et des inversions de l’onde T. Ces caractéristiques communes conduisent souvent à une confusion entre le BBG chronique et le STEMI aigu, entraînant des thrombolyses ou des angiographies inutiles. En fait, des études ont montré que le BBG est la cause la plus fréquente de fausses activations des salles de cathétérisme en urgence.
- Le BBG peut masquer une ischémie en cours : Le BBG provoque une perturbation majeure de la repolarisation ventriculaire. Le vecteur de repolarisation du BBG s’oppose généralement au vecteur QRS. Si un vecteur de lésion ischémique (STEMI) survient, il peut être électriquement « annulé » par le vecteur de repolarisation du BBG. Par conséquent, les modifications ischémiques du segment ST (élévations ST, dépressions ST, modifications de l’onde T) sont généralement dissimulées. Un patient souffrant d’un infarctus aigu du myocarde avec occlusion totale de l’IVA peut donc présenter un ECG avec un aspect de BBG qui semble « habituel » ou non diagnostique.
- Le BBG peut être la conséquence directe d’une ischémie ou d’un infarctus : Bien qu’il existe de nombreuses causes chroniques de BBG (hypertension, cardiomyopathie dilatée, fibrose idiopathique du système de conduction ou maladie de Lenègre), l’infarctus aigu du myocarde peut provoquer un BBG de novo. Ceci est particulièrement vrai pour les infarctus antérieurs étendus qui compromettent la perfusion de la branche gauche via les artères septales (branches de l’interventriculaire antérieure). Ainsi, un infarctus aigu du myocarde peut entraîner un BBG qui, paradoxalement, masque ensuite les modifications ischémiques du segment ST-T sur l’ECG, créant un cercle vicieux diagnostique.
En résumé, le bloc de branche gauche (BBG) peut résulter d’une ischémie myocardique aiguë ou d’un infarctus, l’imiter ou le masquer, ce qui pose d’importants problèmes de diagnostic et de triage. Ces complexités ont historiquement conduit les chercheurs à recommander que tous les patients présentant un BBG et suspectés d’infarctus aigu du myocarde (IAM) soient orientés vers une thérapie de reperfusion urgente, qui à l’époque était principalement une fibrinolyse (Wilner et al.). Leurs conclusions avaient révélé qu’un nombre important de ces patients présentaient une occlusion complète de l’artère coronaire (artère coupable) et que les résultats s’amélioraient lorsqu’ils étaient traités comme des cas de STEMI. Cependant, cette stratégie « tous venants » a montré ses limites à l’ère de l’angioplastie primaire.
Prise en charge du bloc de branche gauche (BBG) chez les patients souffrant d’un syndrome coronarien aigu (SCA)
Pendant de nombreuses années, les lignes directrices européennes (ESC) et nord-américaines (AHA/ACC) ont recommandé de traiter les patients présentant des symptômes d’ischémie myocardique et un bloc de branche gauche (BBG) nouveau (ou présumé nouveau) automatiquement comme des cas de STEMI aigu. Cependant, des études ultérieures et des méta-analyses ont montré que cette approche conduisait à un taux inacceptable d’activations inutiles du laboratoire de cathétérisme, avec souvent des artères coronaires saines ou sans lésion coupable aiguë.
En réponse, les lignes directrices nord-américaines (O’Gara et al.) et européennes ont évolué. Elles indiquent désormais que le BBG nouveau (ou présumé nouveau) ne doit plus être considéré isolément comme un équivalent diagnostique d’infarctus aigu du myocarde (IAM). Au contraire, la décision de revascularisation urgente doit reposer sur un faisceau d’arguments. Les patients qui ont une forte suspicion clinique d’ischémie myocardique continue, indépendamment des résultats de l’ECG ou avant le retour des biomarqueurs (troponine), doivent être traités de la même manière que ceux qui souffrent d’un STEMI évident.
Les critères cliniques d’instabilité qui doivent déclencher une angiographie immédiate en présence d’un BBG incluent :
- Instabilité hémodynamique ou choc cardiogénique.
- Œdème pulmonaire aigu ou insuffisance cardiaque aiguë.
- Douleur thoracique ischémique persistante et réfractaire au traitement médical initial.
- Arythmies ventriculaires menaçantes (TV/FV) ou arrêt cardiaque ressuscité.
De même, les lignes directrices 2023 de la Société européenne de cardiologie (ESC) sur les SCA ont confirmé cette approche : les patients présentant un BBG ou un bloc de branche droit (BBD) et des signes ou symptômes indiquant fortement une ischémie myocardique en cours (notamment les critères de Sgarbossa positifs) doivent être traités comme ayant un STEMI définitif, que le bloc de branche soit ou non déjà documenté (Byrne et al.).
Critères ECG de Sgarbossa pour la détection de l’ischémie en présence d’un bloc de branche gauche (BBG)
Il est évident que les chercheurs ont eu du mal à établir des critères ECG pour diagnostiquer un infarctus aigu du myocarde avec sus-décalage du segment ST (STEMI) en présence d’un bloc de branche gauche (BBG). Les critères les plus utiles et les mieux validés sont ceux mis au point par Sgarbossa et ses collègues (Neeland et al.). Ces critères reposent sur l’identification d’une repolarisation concordante (anormale dans le BBG) ou excessivement discordante.
Les trois critères originaux de Sgarbossa sont (voir Figure 1A) :
- Sus-décalage concordant du segment ST ≥ 1 mm dans n’importe quelle dérivation (l’élévation du ST va dans la même direction que le QRS positif). Ce critère est le plus spécifique (5 points).
- Sous-décalage concordant du segment ST ≥ 1 mm dans les dérivations V1, V2 ou V3 (3 points).
- Sus-décalage discordant du segment ST ≥ 5 mm dans une dérivation où le complexe QRS est négatif (2 points).
Les études montrent qu’un seuil de ≥ 3 points donne une spécificité excellente de 90 à 98 %, ce qui signifie qu’un score positif confirme quasi-certainement l’infarctus. Cependant, la sensibilité est notablement faible (20 à 36 %), ce qui rend les critères peu fiables pour exclure l’infarctus aigu du myocarde. L’absence de critères de Sgarbossa n’élimine pas un STEMI.
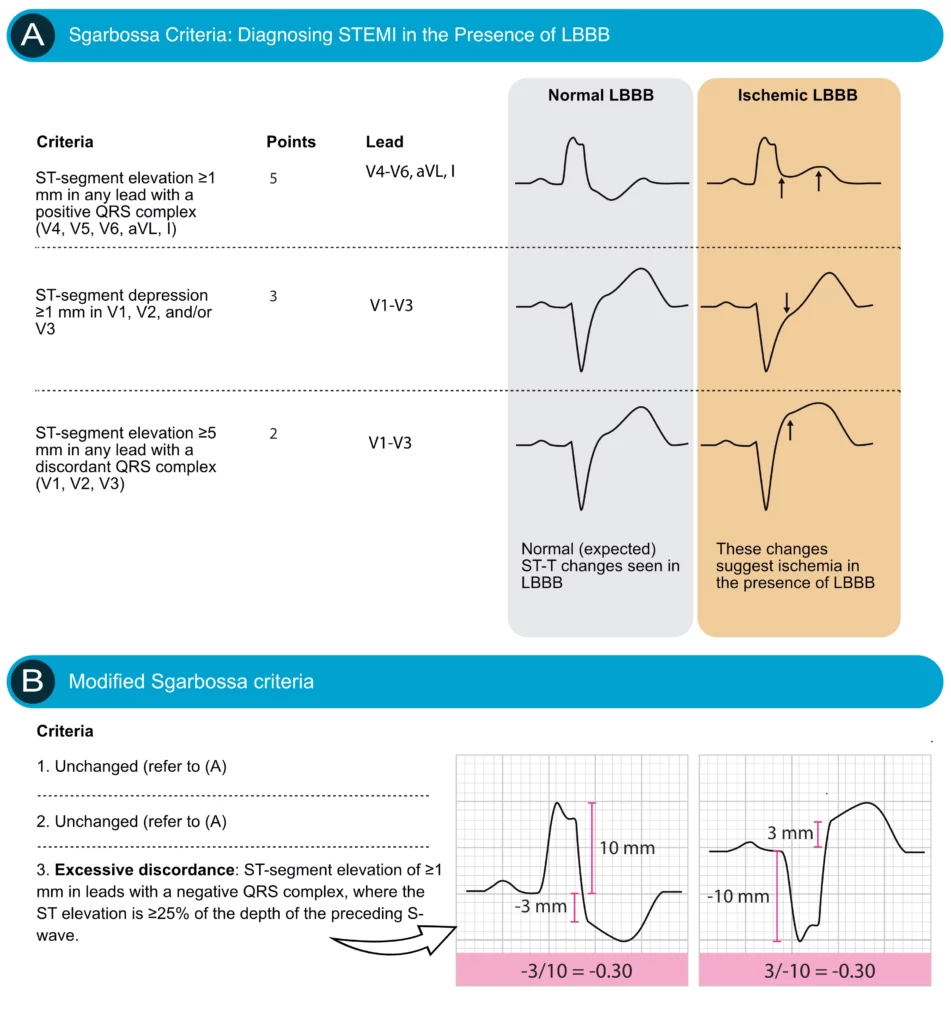
Critères de Sgarbossa modifiés (Critères de Smith)
Le troisième critère original de Sgarbossa (sus-décalage absolu de ≥ 5 mm) s’est avéré problématique car les patients avec un BBG et des ondes S très profondes (HVG importante) peuvent avoir un sus-décalage > 5 mm simplement par discordance appropriée, sans ischémie. À l’inverse, un patient avec de petits voltages peut avoir un infarctus avec seulement 3 ou 4 mm de sus-décalage, ce qui serait manqué par le critère original.
Les critères de Sgarbossa modifiés, introduits par Smith et al. (2012), corrigent cette faiblesse. Ils remplacent le troisième critère absolu par une règle de proportionnalité : un rapport ST/S inférieur à -0,25. La mesure du rapport ST/S est décrite dans la figure 1B. L’utilisation de ce critère améliore considérablement la sensibilité (passant d’environ 30% à près de 80%) tout en maintenant une excellente spécificité. En outre, les critères de Sgarbossa modifiés n’utilisent pas de système de points ; au lieu de cela, il suffit d’un seul des trois critères pour être considéré comme positif (c’est-à-dire qu’une ischémie aiguë est fortement suggérée).
Mesure du rapport ST/S
La méthodologie précise est cruciale pour l’application des critères modifiés :
- Identifiez une dérivation avec un complexe QRS négatif (onde S dominante) et un sus-décalage du segment ST discordant.
- Mesurez l’amplitude de l’onde S (le point le plus bas du QRS) à partir de la ligne isoélectrique (segment PR).
- Mesurez le sus-décalage du segment ST au point J, par rapport au segment PR.
- Calculez le rapport : Amplitude ST / Amplitude S.
Si ce rapport est ≤ -0,25 (c’est-à-dire que le sus-décalage ST représente plus de 25 % de la profondeur de l’onde S), le critère est positif pour un STEMI. Ainsi, les critères modifiés suggèrent d’utiliser une règle de proportionnalité plutôt qu’une valeur absolue ; l’amplitude de la déviation ST est comparée à l’amplitude de l’onde R ou S, ce qui augmente à la fois la sensibilité et la spécificité de l’infarctus aigu du myocarde.

Autres signes ECG d’infarctus en présence d’un BBG
Outre les critères de Sgarbossa, d’autres signes morphologiques plus subtils peuvent orienter vers un diagnostic d’infarctus du myocarde, bien qu’ils soient moins sensibles :
- Signe de Cabrera : Il s’agit d’une encoche (« notch ») présente sur la branche ascendante de l’onde S dans les dérivations V3 ou V4. Ce signe, bien que peu sensible, est très spécifique (90%+) d’un infarctus ancien ou récent de la paroi antérieure.
- Signe de Chapman : Similaire au signe de Cabrera, il correspond à une encoche sur la branche ascendante de l’onde R dans les dérivations V5, V6 ou I.
- Ondes Q pathologiques : En présence d’un BBG, la présence d’ondes Q en I, aVL, V5 ou V6 est hautement anormale et suggère fortement un infarctus (les forces septales initiales étant normalement absentes ou inversées dans le BBG).
Critères d’infarctus chez les patients présentant un BBG, une hypertrophie ventriculaire gauche (HVG) et des rythmes de pacemaker
Les lignes directrices européennes et nord-américaines recommandent de ne pas appliquer les critères ECG standard pour l’ischémie ou l’infarctus en présence d’un bloc de branche gauche (BBG), d’une hypertrophie ventriculaire gauche (HVG) ou d’un rythme de pacemaker ventriculaire. Ces conditions modifient de manière significative le complexe QRS et les formes d’ondes ST-T, pouvant potentiellement imiter ou dissimuler des signes d’ischémie. Toutefois, il est raisonnable d’évaluer les formes d’ondes anormales dans le contexte spécifique du BBG, de l’HVG ou des rythmes stimulés.
Application aux rythmes électro-entraînés (Pacemaker)
La stimulation ventriculaire droite (pacemaker) produit un aspect ECG très similaire au BBG, car l’activation commence dans le ventricule droit et se propage lentement vers le ventricule gauche. Par conséquent, les critères de Sgarbossa (et en particulier les critères modifiés de Smith) sont également applicables et validés pour le diagnostic de l’infarctus du myocarde chez les patients porteurs d’un stimulateur cardiaque entraînant le ventricule droit. Un sus-décalage concordant du ST sous stimulation ventriculaire est un signe d’alerte majeur.
En conclusion, pour maximiser la précision diagnostique :
- Comparez toujours les formes d’ondes ECG actuelles avec les enregistrements précédents afin d’identifier toute différence dynamique. Les variations du segment ST-T peuvent indiquer une ischémie.
- Assurez-vous que les formes d’onde de l’ECG correspondent aux schémas attendus pour l’affection sous-jacente. Par exemple, les inversions de l’onde T dans les dérivations V5, V6, aVL et I sont typiques du bloc de branche gauche non compliqué ; leur absence (ondes T positives concordantes) peut suggérer une ischémie aiguë.
- Recherchez une pseudonormalisation des ondes T, qui peut également être un marqueur d’ischémie transitoire.