Prévision de l’arrêt cardiaque soudain
L’objectif de la découverte et de la mesure des facteurs de risque est d’obtenir des estimations précises, d’adapter la prise en charge thérapeutique et de surveiller l’évolution du risque de manière prospective. Les facteurs de risque majeurs servent de variables indépendantes dans les modèles multivariés de prédiction. Le ciblage des facteurs de risque s’est avéré très efficace dans la prévention primaire et secondaire des maladies cardiovasculaires athérosclérotiques, tant au niveau de la population qu’au niveau individuel. Plusieurs modèles de prédiction (scores de risque) ont été développés et validés pour la prédiction de l’insuffisance cardiaque, de la maladie coronarienne, des syndromes coronariens aigus et des accidents vasculaires cérébraux(Steyerberg et al). Il a été historiquement beaucoup plus difficile d’y parvenir pour la prédiction de l’arrêt cardiaque soudain (ACS) ou de la mort subite cardiaque (MSC).
L’arrêt cardiaque soudain est la manifestation la plus meurtrière des maladies cardiovasculaires, représentant environ 50 % de tous les décès d’origine cardiovasculaire(Tsao et al). Une méta-analyse récente a montré que la survie jusqu’à la sortie de l’hôpital est de seulement 8,8 % et que la survie à 30 jours est de 10,7 % en cas d’arrêt cardiaque extrahospitalier, souvent avec des séquelles neurologiques majeures(Yan et al). Ce faible taux de survie reflète la nature soudaine, hyperaiguë et souvent inaugurale de l’arrêt cardiaque. Cela a incité les chercheurs à développer des stratégies et des outils pour la prévention à long terme (implantation de défibrillateurs, modulation du substrat). Malheureusement, en dehors de populations à très haut risque bien définies, ces efforts n’ont pas encore permis d’éradiquer le problème à l’échelle populationnelle. Notre capacité actuelle à prédire l’arrêt cardiaque chez l’individu asymptomatique reste limitée.
L’une des principales explications est la nature stochastique de l’arrêt cardiaque soudain et de la mort. Le caractère aléatoire de l’événement intrigue les chercheurs depuis plus de 80 ans. C’est ce qu’ont exprimé Beck et al en 1961 dans le Journal of American Medical Association (JAMA), soulignant la distinction entre le cœur « malade » anatomiquement et le cœur « électriquement instable » :
[…] Sur 10 victimes de ce type, le cœur de 6 ou 7 d’entre elles ne présentait aucune maladie récente des artères coronaires ou du muscle cardiaque. En d’autres termes, le cœur d’aujourd’hui est anatomiquement le même que celui d’hier, si ce n’est qu’une charge électrique s’est développée et a entraîné la fibrillation du cœur. Ce facteur électrique est venu, a tué et a disparu et n’a pas été retrouvé dans le cœur mort. La cause de la mort de ces victimes n’est pas expliquée sur la base d’une anatomie morbide. Cette expérience n’est pas nouvelle pour le pathologiste ou l’interniste. Le fait que nous ne comprenions pas bien ce problème est mis en évidence lorsque le décès survient alors que la victime avait reçu un “certificat de bonne santé” et qu’aucune explication n’avait été donnée […]
Ce n’est que dans un petit sous-groupe de patients très sélectionnés (principalement avec une fraction d’éjection altérée ou des canalopathies identifiées) que des prévisions raisonnables peuvent être faites, guidant les décisions concernant l’implantation de DAI (défibrillateur automatique implantable) en prévention primaire. Notre incapacité à prédire les arrêts cardiaques dans la population générale est évidente à bien des égards :
- Les DAI modernes sont capables de défibriller avec succès 99 % des tachyarythmies ventriculaires. Théoriquement, les DAI pourraient traiter la quasi-totalité des arrêts cardiaques causés par des tachyarythmies ventriculaires (FV/TV). Pourtant, seule une fraction négligeable des victimes d’arrêts cardiaques dans la population générale est porteuse d’un DAI au moment de l’événement.
- La moitié des victimes d’arrêts cardiaques n’ont aucun antécédent connu de maladie cardiovasculaire avant l’événement fatal. La mort subite d’origine cardiaque représente 40 à 70 % de tous les décès dus à une maladie coronarienne (Kannel et al., Demirovic et al.), et est souvent le premier et dernier symptôme.
Comme le décrivent Myerburg et al. et Marijon et al., la prévention à long terme des arrêts cardiaques au niveau de la population est un défi épidémiologique majeur. Les efforts futurs pourraient être plus fructueux en se concentrant sur la prédiction à court terme à l’aide d’appareils connectés (wearables), de l’intelligence artificielle appliquée à l’ECG et de technologies émergentes permettant de détecter l’instabilité électrique imminente (Marijon et al.).
Le concept de la « Tempête Parfaite »
La nature stochastique (aléatoire) de l’arrêt cardiaque soudain est, par certains aspects, similaire aux syndromes coronariens aigus. Un syndrome coronarien aigu est le résultat d’un scénario de « tempête parfaite », où la rupture ou l’érosion d’une plaque d’athérosclérose vulnérable coïncide avec un moment pro-thrombogène systémique (activation plaquettaire, facteurs de coagulation, dysfonction endothéliale, inflammation). La tempête parfaite implique que la rupture de la plaque survient lorsque les facteurs pro-thrombogènes l’emportent sur les facteurs pro-thrombolytiques endogènes.
L’équilibre entre les facteurs pro-thrombogènes et pro-thrombolytiques détermine la survenue d’une athérothrombose, et ces facteurs varient d’une minute à l’autre. Seule une minorité des ruptures de plaque entraîne un syndrome coronarien aigu clinique ; la majorité des ruptures de plaque sont asymptomatiques et cicatrisent silencieusement (Arbab-Zadeh et al.). L’émergence des tachyarythmies ventriculaires malignes suit les mêmes principes, où les facteurs pro-arythmogènes sont contrés par des facteurs anti-arythmogènes. L’interaction complexe entre le substrat anatomique (cicatrice, fibrose, hypertrophie) et les gâchettes fonctionnelles (extrasystoles, ischémie aiguë, désordres électrolytiques, tonus sympathique, allongement du QT) détermine la survenue de l’arythmie.
Les processus multifactoriels qui aboutissent à un arrêt cardiaque soudain nécessitent généralement l’acquisition d’un substrat arythmogène, capable de générer et de maintenir des tachyarythmies dans des conditions spécifiques (souvent transitoires), comme le montre la figure 1.
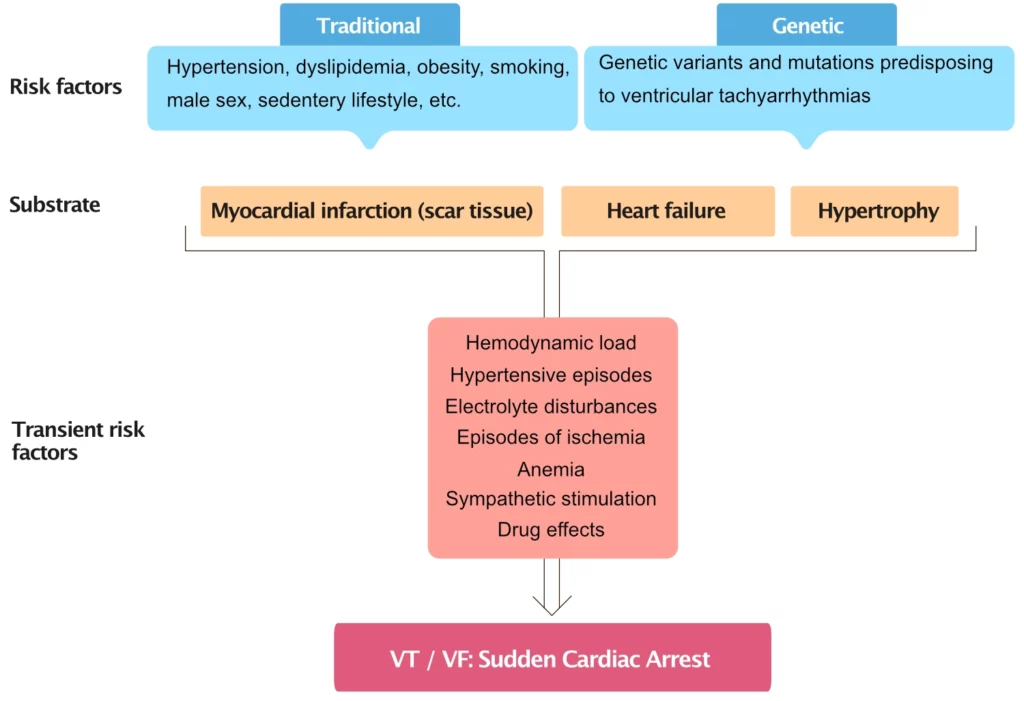
Facteurs de risque cardiovasculaire traditionnels
Les facteurs de risque cardiovasculaire traditionnels (diabète, hypertension artérielle, dyslipidémie, tabagisme, sédentarité, obésité abdominale, etc.) jouent un rôle prépondérant dans la genèse du substrat ischémique. Le risque d’arrêt cardiaque soudain est clairement associé au nombre et à la sévérité de ces facteurs de risque. Les participants du décile le plus à risque de l’étude de Framingham avaient un risque de mort subite cardiaque multiplié par 14 par rapport au décile le moins à risque. Ces facteurs favorisent le développement de la plaque d’athérome, de l’hypertrophie ventriculaire gauche (HVG) et de la fibrose interstitielle, créant ainsi les conditions anatomiques (substrats) propices aux arythmies ventriculaires malignes.
Ces facteurs de risque ont été ciblés avec succès par la prévention primaire, qui a probablement réduit l’incidence globale des arrêts cardiaques en diminuant l’incidence et la gravité de l’infarctus aigu du myocarde (Nabel et al). Néanmoins, l’augmentation de la prévalence de l’obésité et du diabète de type 2 pourrait ralentir ces progrès.
Discordance entre le risque relatif et le risque absolu : Le Paradoxe de Myerburg
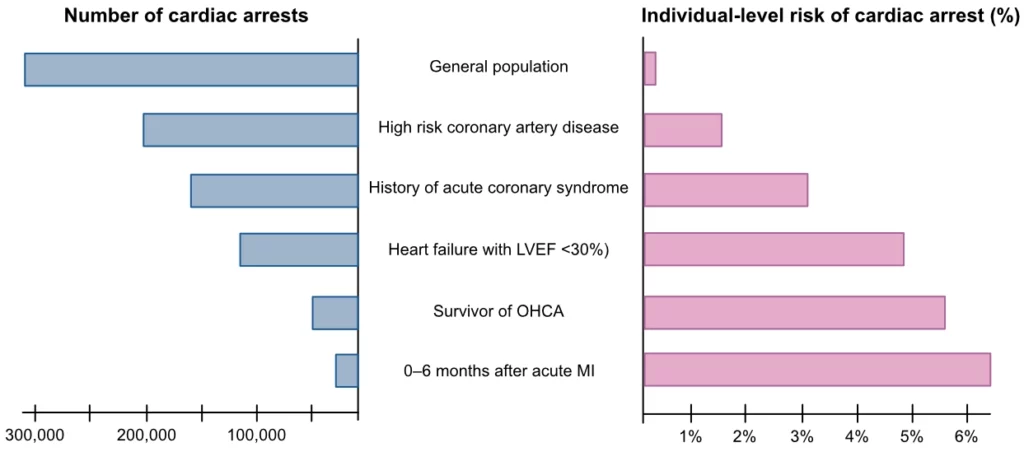
La discordance marquée entre le risque individuel relatif et la fraction attribuable à la population (FAP) constitue l’un des défis majeurs pour identifier les personnes à haut risque. La figure 2 (adaptée de Myerburg et al.) illustre ce phénomène, connu sous le nom de « Paradoxe de Myerburg ». Elle montre que la grande majorité des arrêts cardiaques en nombre absolu surviennent dans la population générale ou chez des patients à risque intermédiaire, dont le risque relatif individuel d’arrêt cardiaque est faible.
Le risque relatif d’arrêt cardiaque étant très faible dans la population générale (environ 0,1 % par an), le nombre total d’arrêts cardiaques dans ce vaste groupe dépasse de loin le nombre d’arrêts dans les groupes à très haut risque (comme les patients post-infarctus avec FEVG < 30%). Ces derniers présentent un risque relatif individuel extrêmement élevé, justifiant l’implantation de DAI, mais ne comptent que pour une minorité des cas totaux en raison de la petite taille de cette sous-population.
Aperçu des facteurs de risque d’arrêt cardiaque
- Âge – La courbe d’incidence est bimodale : le risque est élevé au cours de la première année de vie (SMSN) et augmente de façon exponentielle après 45 ans. À partir de 35 ans, la maladie coronarienne est la cause prédominante.
- Sexe masculin – Les hommes courent un risque plus élevé d’arrêt cardiaque que les femmes tout au long de leur vie (ratio environ 3:1). Cependant, la proportion de femmes augmente après la ménopause.
- Variations circadiennes – Le risque d’arrêt cardiaque suit un rythme circadien avec un pic matinal (au réveil), souvent associé à l’augmentation des catécholamines et du tonus sympathique. On note aussi une incidence accrue le lundi et pendant les mois d’hiver.
- Environnement et Toxiques – La pollution atmosphérique (particules fines) augmente le risque d’infarctus aigu et d’arythmie. La consommation de cocaïne et d’autres stimulants est une cause croissante d’ACS chez les sujets jeunes.
- Maladie cardiovasculaire établie – Les personnes souffrant d’une maladie coronarienne, d’insuffisance cardiaque (ischémique ou non), de cardiomyopathie hypertrophique ou dilatée, ou de cardiopathie valvulaire présentent un risque accru. En phase aiguë d’infarctus du myocarde, le risque de fibrillation ventriculaire (FV) est maximal au cours de la première heure.
- Facteurs métaboliques – L’hypertension (cause d’HVG), le diabète (neuropathie autonome et athérosclérose diffuse), l’apnée du sommeil (hypoxie intermittente), l’obésité et la dyslipidémie sont des contributeurs majeurs.
- La consommation d’alcool présente une courbe en J : une consommation modérée pourrait réduire légèrement le risque via la protection coronarienne, mais une consommation excessive (binge drinking ou chronique) augmente le risque de cardiomyopathie alcoolique et d’arythmies (« Holiday Heart Syndrome »).
- Génétique et Canaloathies – Le syndrome de Brugada, le syndrome du QT long congénital, le syndrome du QT court, la tachycardie ventriculaire polymorphe catécholaminergique (TVPC) et la cardiomyopathie arythmogène du ventricule droit (CAVD) sont des causes classiques de mort subite chez le sujet jeune (< 35 ans). L’autopsie moléculaire joue un rôle crucial pour dépister les familles en cas de décès inexpliqué.
Fraction d’éjection du ventricule gauche (FEVG)
Le lien étroit entre la fraction d’éjection du ventricule gauche (FEVG) et le risque d’arrêt cardiaque soudain est reconnu depuis des décennies et reste la pierre angulaire de la stratification du risque actuelle (Bigger et al.). Une FEVG basse reflète l’étendue des dommages myocardiques et le remodelage pathologique. Les essais historiques (MADIT-II, SCD-HeFT) ont démontré que l’implantation d’un DAI en prévention primaire chez les personnes ayant une FEVG ≤ 30-35 % (après infarctus ou dans les cardiomyopathies dilatées) réduisait significativement la mortalité totale et la mort subite.
Cependant, des recommandations basées uniquement sur la FEVG présentent des limites importantes :
- Sensibilité insuffisante : La majorité des arrêts cardiaques surviennent chez des patients ayant une FEVG > 35 % (zone grise ou fonction préservée), qui ne sont pas éligibles au DAI selon les critères actuels.
- Spécificité limitée : La FEVG est un indicateur imparfait du mode de décès. Chez les patients en insuffisance cardiaque avancée (NYHA III-IV), bien que la mortalité totale soit élevée, le décès est souvent dû à une défaillance de pompe (choc cardiogénique) plutôt qu’à une arythmie, ce qui réduit le bénéfice relatif du DAI par rapport aux patients moins symptomatiques (NYHA I-II) où la mort subite prédomine proportionnellement (Packer et al.).
- Variabilité de la mesure : L’échocardiographie, bien que largement disponible, est opérateur-dépendante. L’IRM cardiaque offre une précision supérieure.
Au-delà de la FEVG : L’imagerie et le substrat cicatriciel
Pour améliorer la prédiction, l’évaluation du substrat arythmogène est essentielle. L’imagerie par résonance magnétique (IRM) cardiaque avec injection de gadolinium permet de détecter et quantifier le rehaussement tardif (Late Gadolinium Enhancement – LGE). Ce rehaussement correspond aux zones de fibrose ou de cicatrice myocardique.
La présence de fibrose, qu’elle soit d’origine ischémique (cicatrice d’infarctus) ou non ischémique (fibrose interstitielle ou de remplacement dans les cardiomyopathies dilatées ou hypertrophiques), est un puissant prédicteur indépendant d’arythmies ventriculaires. La cicatrice crée des zones de conduction lente et des blocs unidirectionnels, favorisant les circuits de réentrée, mécanisme principal des tachycardies ventriculaires monomorphes.
Autres facteurs de risque et marqueurs électrophysiologiques
La stratification du risque s’enrichit de marqueurs non invasifs reflétant l’instabilité électrique et le déséquilibre du système nerveux autonome :
- ECG de repos : L’allongement de l’intervalle QTc, la dispersion du QT, les ondes T négatives géantes, le bloc de branche gauche (BBG) et le QRS fragmenté (signe de cicatrice) sont des marqueurs de risque. Le repolarisation précoce dans les dérivations inférieures/latérales est également associée à un risque accru de FV idiopathique.
- Variabilité de la fréquence cardiaque (VFC) : Une réduction de la VFC, signe d’un tonus vagal diminué et d’une dominance sympathique, est associée à une mortalité accrue post-infarctus.
- Alternance de l’onde T (T-wave Alternans) : La variation microvoltée de l’amplitude de l’onde T d’un battement à l’autre reflète une instabilité de la repolarisation et une vulnérabilité à la FV.
- Capacité d’exercice : Une faible capacité fonctionnelle et une récupération lente de la fréquence cardiaque après l’effort (défaut de réactivation vagale) sont des prédicteurs de mortalité.
- Activité physique et risque paradoxal : Le risque de subir un arrêt cardiaque pendant une activité physique vigoureuse est transitoirement élevé, surtout chez les sujets non entraînés (RR > 50). Cependant, l’entraînement régulier réduit considérablement le risque global à long terme. Les sédentaires doivent augmenter leur charge d’exercice progressivement.
- Troubles du rythme ventriculaire :
- Les extrasystoles ventriculaires (ESV) fréquentes (>10-30/h) ou polymorphes.
- La tachycardie ventriculaire (TV) non soutenue : son importance pronostique dépend du contexte (bénigne sur cœur sain, péjorative sur cœur structurellement atteint, notamment dans la cardiomyopathie hypertrophique).
- La TV inductible lors de l’exploration électrophysiologique reste un critère majeur dans certaines indications post-infarctus.
Références
Myerburg RJ, Junttila MJ. Sudden cardiac death caused by coronary heart disease. Circulation. 2012.
Myerburg RJ, Castellanos A. Arrêt cardiaque et mort cardiaque subite. Man DL, Zipes DP, Libby P, Bonow RO. Braunwald’s Heart Disease : A Textbook of Cardiovascular Medicine. 10e éd. Elsevier.
Myerburg RJ, Kessler KM, Castellanos A. Sudden cardiac death : structure, function, and time-dependence of risk. Circulation 1992;85(suppl I):1-2,1-10.
Yoshinaga M, Kucho Y, Nishibatake M, et al. Probabilité de diagnostic du syndrome du QT long chez les enfants et les adolescents selon les critères de la déclaration de consensus d’experts HRS/EHRA/APHRS. Eur Heart J. 2016.
Nabel EG, Braunwald E. A Tale of Coronary Artery Disease and Myocardial Infarction. N Engl J Med 2012; 366:54-63.
Albert CM, Mittleman MA, Chae CU, et al. Triggering of sudden death from cardiac causes by vigorous exertion. N Engl J Med. 2000.
Chugh SS, Reinier K, Singh T, et al. Determinants of prolonged QT interval and their contribution to sudden death risk in coronary artery disease: The Oregon Sudden Unexpected Death Study. Circulation. 2009.
Steyerberg EW, Vergouwe Y. Towards better clinical prediction models: seven steps for development and an ABCD for validation. European Heart Journal, 2014.
Demirovic J. Facteurs de risque dans l’incidence de la mort cardiaque subite et possibilités de prévention. Thèse de doctorat, University of Belgrade Press, Belgrade, YU. 1985.
Myerburg RJ. Implantable cardioverter-defibrillators after myocardial infarction. N Engl J Med. 2008.
Goldberger JJ, Buxton AE, Cain M, et al. Risk stratification for arrhythmic sudden cardiac death: identifying the roadblocks. Circulation. 2011.
Bigger JT, Fleiss JL, Kleiger R, Miller JP, Rolnitzky LM. The relationships among ventricular arrhythmias, left ventricular dysfunction, and mortality in the 2 years after myocardial infarction. Circulation 1984;69:250-258.
Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, et al. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction (MADIT-II). N Engl J Med 2002;346:877-883.
Packer M. Competing risks and the clinical progression of heart failure. Circulation 2004.
Tsao CW, Aday AW, Almarzooq ZI, et al. Heart Disease and Stroke Statistics—2022 Update: A Report From the American Heart Association. Circulation 2022.