Introduction à l’interprétation de l’ECG pédiatrique et néonatal
Principes de l’interprétation de l’ECG pédiatrique et néonatal
- Spécificités techniques de l’enregistrement
- Développement physiologique et anatomique pendant la petite enfance et l’enfance
- La circulation fœtale
- La circulation postnatale
- Évolution des intervalles et de la morphologie ECG
- Valeurs normales (valeurs de référence) pour l’ECG chez les patients néonatals et pédiatriques
- Indications pour l’ECG chez les enfants (patients néonatals et pédiatriques)
L’interprétation de l’ECG pédiatrique et néonatal suit les mêmes principes électrophysiologiques fondamentaux que l’interprétation de l’ECG chez l’adulte, mais il existe des différences cliniques majeures. Ces distinctions s’expliquent en grande partie par les changements physiologiques et anatomiques profonds qui se produisent pendant la période néonatale, la petite enfance et l’adolescence. Les modifications les plus marquées surviennent au cours de la première année de vie, reflétant l’adaptation cardio-circulatoire à la vie extra-utérine. L’électrocardiogramme (ECG) évolue donc parallèlement aux changements anatomiques, hémodynamiques et physiologiques du cœur. Les amplitudes, les axes, les intervalles et la morphologie des ondes de l’ECG sont substantiellement différents chez les enfants par rapport aux adultes, avec des variations continues en fonction de l’âge (nomogrammes). Les cliniciens qui travaillent dans le domaine des soins pédiatriques et néonatals doivent impérativement maîtriser ces variations physiologiques (« moving target ») pour éviter de pathologiser un tracé normal, ainsi que connaître les cardiopathies congénitales et acquises spécifiques à cette population.
Spécificités techniques de l’enregistrement
La réalisation technique de l’ECG chez le nourrisson et le petit enfant requiert une attention particulière. La surface corporelle réduite impose un placement précis des électrodes pour éviter le chevauchement des signaux. De plus, l’agitation de l’enfant peut créer des artefacts musculaires importants.
Il est souvent nécessaire d’enregistrer des dérivations supplémentaires. Étant donné la prédominance du ventricule droit chez le nouveau-né et le nourrisson, l’utilisation des dérivations droites (V3R et V4R) est fréquemment indiquée pour mieux explorer le myocarde ventriculaire droit. La vitesse de défilement du papier est standard (25 mm/s), mais peut être augmentée à 50 mm/s pour mieux analyser les tachyarythmies rapides, fréquentes chez l’enfant.
Développement physiologique et anatomique pendant la petite enfance et l’enfance
Chez l’adulte sain, le ventricule gauche est considérablement plus massif que le ventricule droit. C’est le résultat de l’adaptation ventriculaire aux résistances vasculaires respectives. Le ventricule gauche doit surmonter la pression systémique (post-charge), générant une pression systolique d’environ 120 mmHg. Le ventricule droit, quant à lui, éjecte contre la circulation pulmonaire à basse pression (environ 15-25 mmHg de pression systolique). La résistance vasculaire systémique étant plusieurs fois supérieure à la résistance vasculaire pulmonaire, la masse musculaire du ventricule gauche devient prépondérante avec l’âge. Reportez-vous à la figure 1.
«
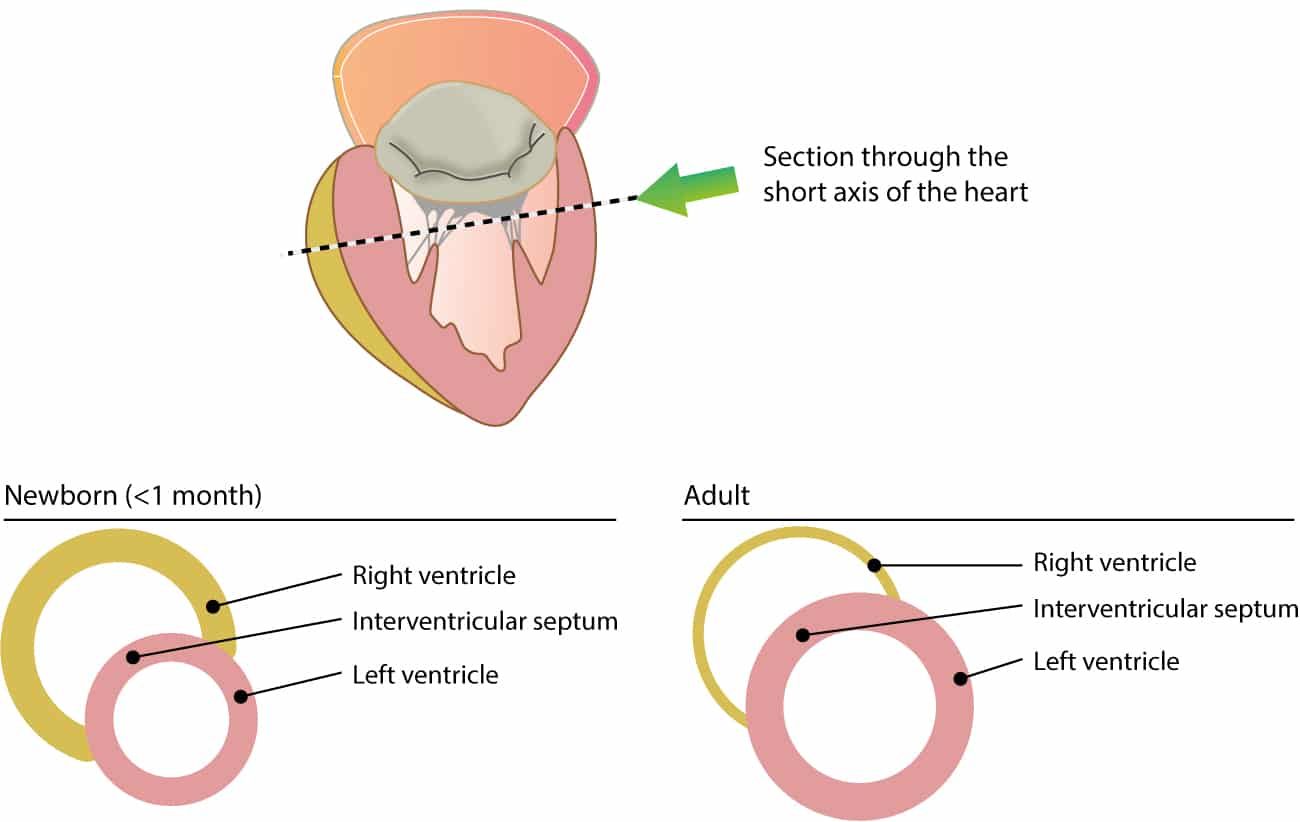
Cette dominance ventriculaire gauche chez l’adulte se traduit électriquement par des complexes QRS dominés par les vecteurs de force du ventricule gauche. Ainsi, les dérivations précordiales gauches (V4-V6) présentent normalement de grandes ondes R et les dérivations droites (V1-V2) des ondes S profondes (voir L’ECG normal). À l’inverse, l’ECG néonatal reflète la prédominance droite.
La circulation fœtale
Pendant la vie intra-utérine et le premier mois de vie postnatale, la physiologie est inversée : le ventricule droit est dominant et sa paroi est plus épaisse que celle du ventricule gauche. Cela s’explique par l’hémodynamique fœtale particulière illustrée à la figure 2.
Le fœtus reçoit du sang oxygéné du placenta via la veine ombilicale et la veine cave inférieure. Ce sang pénètre dans l’oreillette droite. Parallèlement, le sang désoxygéné venant de la partie supérieure du corps (via la veine cave supérieure) arrive aussi dans l’oreillette droite. Grâce aux structures fœtales, les flux sont dirigés préférentiellement :
- Le Foramen Ovale : La majeure partie du sang oxygéné venant de la veine cave inférieure est dirigée directement vers l’oreillette gauche via le foramen ovale, puis vers le ventricule gauche et l’aorte ascendante pour perfuser le cerveau et le cœur (coronaires).
- Le Canal Artériel : Le sang venant du ventricule droit est éjecté dans l’artère pulmonaire. Cependant, les poumons fœtaux étant collabés et remplis de liquide, les résistances vasculaires pulmonaires sont très élevées. Par conséquent, la majorité du débit ventriculaire droit passe par le canal artériel vers l’aorte descendante, contournant ainsi la circulation pulmonaire.
Dans cette configuration, le ventricule droit travaille contre une résistance systémique (via le canal artériel) et pulmonaire élevée. Il assure environ 2/3 du débit cardiaque combiné fœtal. Cette surcharge en pression explique l’hypertrophie physiologique du ventricule droit à la naissance.
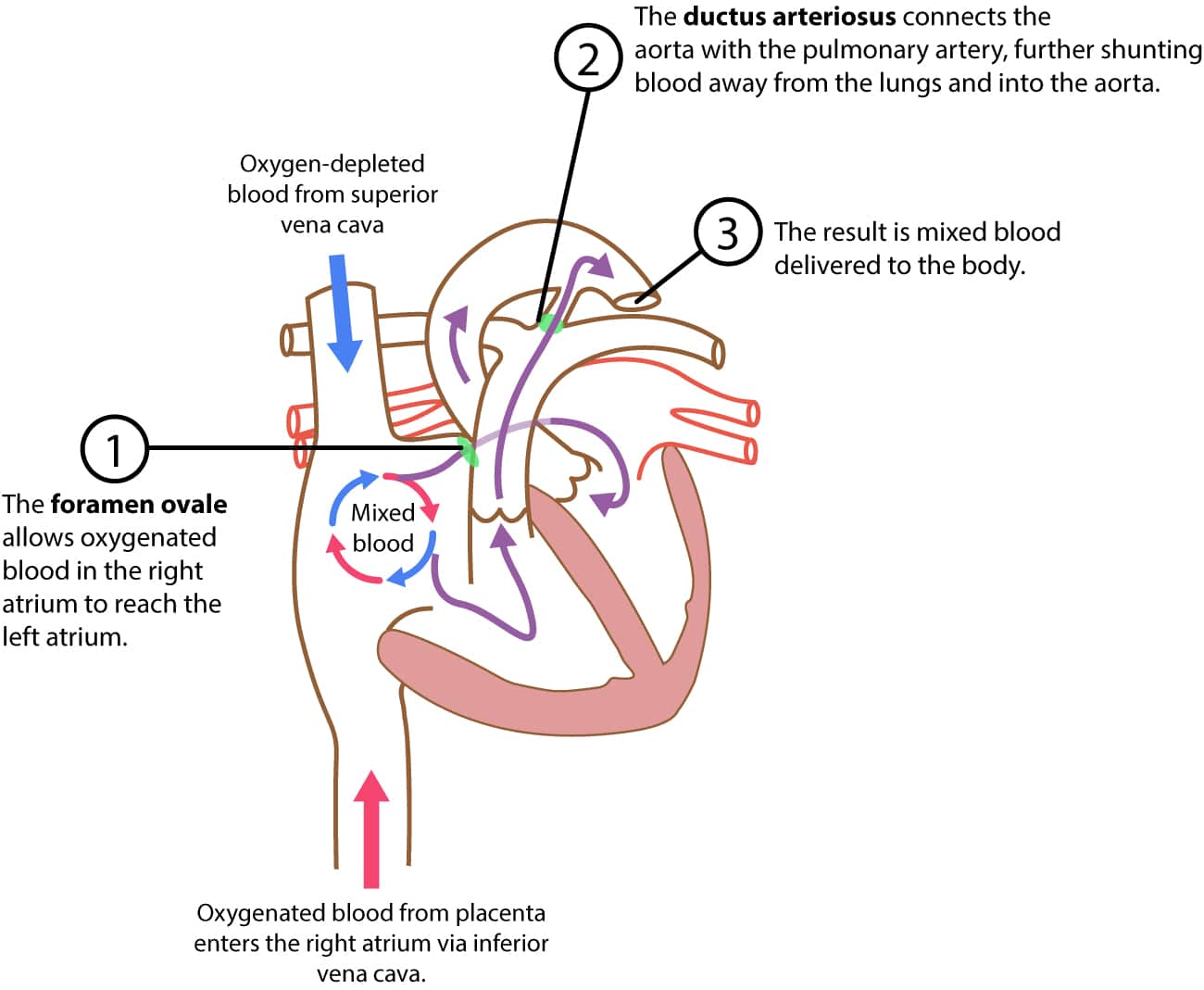
Sur l’ECG du nouveau-né, cette dominance ventriculaire droite se traduit par :
- Un axe QRS dévié à droite (généralement > +90°).
- Des ondes R amples et exclusives en V1 (aspect R pur ou qR).
- Des ondes S profondes en V6.
La circulation postnatale
À la naissance, l’expansion pulmonaire et l’oxygénation entraînent une chute brutale des résistances vasculaires pulmonaires. Simultanément, la suppression de la circulation placentaire augmente les résistances systémiques. Ces changements de pression inversent les gradients :
«
- Le débit pulmonaire augmente massivement, augmentant le retour veineux vers l’oreillette gauche. La pression dans l’oreillette gauche dépasse celle de l’oreillette droite, plaquant le septum primum contre le septum secundum : c’est la fermeture fonctionnelle du foramen ovale.
- L’augmentation de l’oxygène artériel et la chute des prostaglandines provoquent la vasoconstriction puis la fermeture du canal artériel (fonctionnelle en 10-15 heures, anatomique en quelques jours/semaines).
- Le ventricule gauche commence à s’hypertrophier pour faire face à l’augmentation de la post-charge systémique, tandis que le ventricule droit s’affine relativement.
L’évolution ECG suit cette remodelage : à l’âge d’un mois, le ventricule gauche commence à prédominer. Vers 6 mois, le rapport de masse VG/VD se rapproche de celui de l’adulte, bien que des signes de « dominance droite » relative (ondes R plus amples en précordiales droites) puissent persister physiologiquement durant l’enfance.
Note clinique importante : L’hypoxie, l’acidose ou l’hypothermie néonatale peuvent maintenir une vasoconstriction pulmonaire, causant une Hypertension Pulmonaire Persistante du Nouveau-né (HTPPN). Cela maintient le shunt droit-gauche par le foramen ovale ou le canal artériel, entraînant une cyanose réfractaire. L’ECG montrera alors une persistance ou une aggravation des signes d’hypertrophie ventriculaire droite.
Évolution des intervalles et de la morphologie ECG
Fréquence cardiaque et conduction
La fréquence cardiaque au repos est nettement plus élevée chez le nouveau-né (110-150 bpm) et diminue progressivement avec l’âge pour atteindre les valeurs adultes à l’adolescence. Cette fréquence élevée, combinée à une masse myocardique plus faible, raccourcit tous les intervalles de conduction.
- Intervalle PR : Plus court chez l’enfant (80-110 ms chez le nouveau-né) et s’allonge avec l’âge et la diminution de la fréquence cardiaque.
- Durée du complexe QRS : Reflète le temps de dépolarisation ventriculaire. Il est très court chez le prématuré et le nouveau-né (environ 50-70 ms) et augmente progressivement (atteignant 80-100 ms chez l’adolescent) à mesure que la masse myocardique augmente. Un QRS > 80 ms chez un nouveau-né peut déjà indiquer un trouble de conduction ou une hypertrophie ventriculaire majeure.
- Intervalle QT : Il doit toujours être corrigé en fonction de la fréquence cardiaque (QTc). Bien que le QT absolu soit court en raison de la tachycardie, le QTc reste relativement constant, avec une limite supérieure normale légèrement plus élevée chez le nourrisson (jusqu’à 450-460 ms) que chez l’adulte.
Axe du cœur et progression de l’onde R/S
L’évolution de l’axe du QRS dans le plan frontal est un marqueur clé de la maturation cardiaque :
- Nouveau-né : Axe droit marqué (+90° à +180°).
- 1 an : L’axe se verticalise (+60° à +90°).
- Enfant/Adolescent : L’axe devient normal, intermédiaire (0° à +90°).
Parallèlement, dans les dérivations précordiales, on observe une régression de l’onde R en V1 (reflet du VD) et une croissance de l’onde R en V6 (reflet du VG). Le ratio R/S en V1 est > 1 chez le nourrisson et devient < 1 chez l'enfant plus âgé (généralement après 2-3 ans).
La dynamique de l’onde T (Repolarisation)
L’onde T subit des changements caractéristiques qu’il est crucial de ne pas interpréter comme une ischémie :
- À la naissance : L’onde T est positive en V1.
- J3 – J7 : L’onde T s’inverse en V1 (devient négative). Si l’onde T reste positive en V1 après le 7ème jour, cela peut être un signe d’hypertrophie ventriculaire droite pathologique.
- Enfance : L’onde T reste négative de V1 à V3 (parfois V4). C’est le modèle juvénile de l’onde T.
- Adolescence : L’onde T se positive progressivement dans les précordiales droites, bien qu’une onde T négative isolée en V1 puisse persister chez l’adulte (variant normal).
La figure 3 présente un ECG enregistré chez une fille de 8 jours. L’axe électrique dévie vers la droite (QRS négatif dans la dérivation I et QRS positif dans la dérivation II). Les ondes R sont proéminentes dans les dérivations V1, V2 et V3. Il y a des ondes T négatives dans V1-V3, ce qui est attendu à cet âge (après la première semaine). Il y a des ondes Q fines et profondes dans les dérivations inférieures (II, aVF, III) et latérales (V5, V6), courantes en pédiatrie.
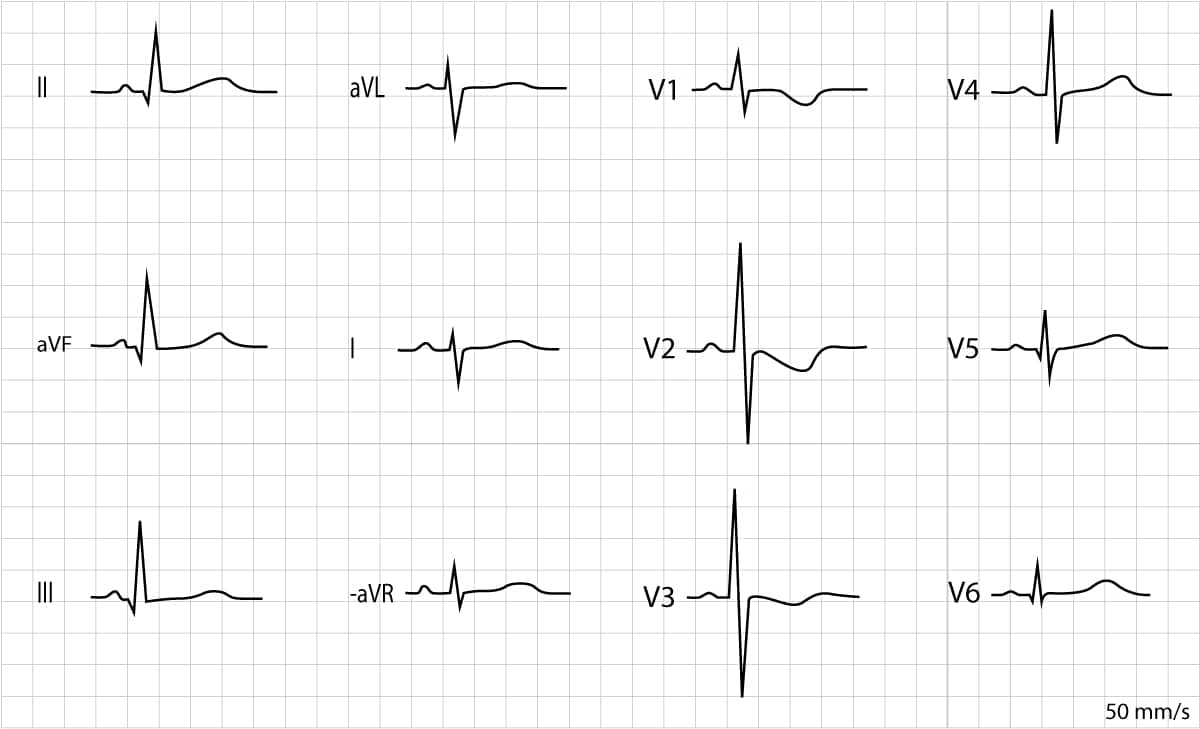
Valeurs normales (valeurs de référence) pour l’ECG chez les patients néonatals et pédiatriques
L’interprétation ne peut se faire sans comparaison à des normes établies par tranche d’âge. Il existe peu de bases de données complètes récentes. Les cliniciens utilisent traditionnellement les valeurs normales publiées en 1979 par Davignon et al et en 2001 par Rijnbeek et al. La Société européenne de cardiologie recommande d’utiliser les valeurs normales publiées par Davignon et al pour l’interprétation de l’ECG néonatal, car Rijnbeek et al n’ont pas inclus suffisamment d’enfants de moins de 30 jours. Pour les enfants âgés de 30 jours ou plus, les deux référentiels sont acceptables. L’utilisation de percentiles (P2 et P98) est indispensable pour déterminer les limites pathologiques de la fréquence, de l’axe, des durées (QRS, QT) et des voltages (indices d’hypertrophie).
Indications pour l’ECG chez les enfants (patients néonatals et pédiatriques)
Les indications de l’ECG pédiatrique sont larges et couvrent le diagnostic des arythmies, le dépistage des cardiopathies congénitales et le suivi systémique :
- Symptômes cliniques : Syncope, quasi-syncope, palpitations, douleurs thoraciques (surtout à l’effort), cyanose, dyspnée inexpliquée.
- Signes physiques : Souffle cardiaque, bruits du cœur anormaux, anomalies du pouls fémoral (coarctation), hypertension artérielle.
- Troubles du rythme suspectés : Tachycardie inexpliquée, bradycardie, irrégularités du rythme.
- Contexte aigu : Crises convulsives (diagnostic différentiel avec syncope ou QT long), hypothermie, déséquilibre électrolytique (kaliémie, calcémie), intoxication médicamenteuse (antidépresseurs tricycliques, etc.).
- Pathologies systémiques et inflammatoires : Maladie de Kawasaki (anévrismes coronaires, ischémie), rhumatisme articulaire aigu (allongement PR), péricardite, myocardite.
- Suivi post-opératoire : Après correction de cardiopathie congénitale (surveillance des blocs auriculo-ventriculaires ou arythmies cicatricielles).
- Dépistage familial : Antécédents familiaux de mort subite, de cardiomyopathie hypertrophique ou de canalopathies (QT long, Brugada).